题目内容
9.以下说法正确的是( )| A. | C60与金刚石一样属于原子晶体 | |
| B. | 干冰升华破坏了共价键 | |
| C. | 共价化合物中一定不含离子键 | |
| D. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 |
分析 A.C60为分子晶体;
B.干冰为分子晶体;
C.含有离子键的化合物为离子化合物;
D.氯化氢为共价化合物.
解答 解:A.C60为分子晶体,金刚石为原子晶体,故A错误;
B.干冰为分子晶体,升华克服分子间作用力,故B错误;
C.含有离子键的化合物为离子化合物,共价键不含离子键,故C正确;
D.氯化氢为共价化合物,且为电解质,溶于水电离,故D错误.
故选C.
点评 本题考查了化学键和化合物的关系,为高频考点,根据物质的构成微粒及物质的性质来分析解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )
| A. | 丙烷与氯气在光照条件下生成氯丙烷 | |
| B. | 乙烯与溴的四氯化碳溶液反应生成1,2二溴乙烷 | |
| C. | 乙烯与水反应生成乙醇 | |
| D. | 乙烯自身聚合生成聚乙烯 |
20.在四个不同容器中,不同条件下进行合成氨反应.根据在相同时间内测定的结果判断生成氨的速率最快的是( )
| A. | v(N2)=0.1mol•L-1•s-1 | B. | v(H2)=0.1mol•L-1•min-1 | ||
| C. | v(NH3)=0.15mol•L-1•min-1 | D. | v(H2)=0.3mol•L-1•min-1 |
17.已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F原子的电子排布式1s22s22p63s23p63d64s2,F位于周期表第VIII族.
(2)A、B、C的第一电离能由小到大的顺序为C<O<N.
(3)F和M(质子数为25)两元素的部分电离能数据列于如表:
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.你的解释是Mn2+的3d轨道电子排布为半满状态较稳定.
(4)已知F晶体的堆积方式与金属钾相同,则F晶胞中F原子的配位数为8,一个晶胞中F原子的数目为2.
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因H2O2分子间存在氢键,与水分子可形成氢键.
(1)写出F原子的电子排布式1s22s22p63s23p63d64s2,F位于周期表第VIII族.
(2)A、B、C的第一电离能由小到大的顺序为C<O<N.
(3)F和M(质子数为25)两元素的部分电离能数据列于如表:
| 元 素 | M | F | |
| 电能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(4)已知F晶体的堆积方式与金属钾相同,则F晶胞中F原子的配位数为8,一个晶胞中F原子的数目为2.
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
4.向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴加几滴溴水后,混合液出现血红色.那么,由此得出下列的结论错误的是( )
| A. | 该晶体中一定含有SCN- | |
| B. | Fe3+的氧化性比Br2的氧化性强 | |
| C. | Fe2+被Br2氧化为Fe3+ | |
| D. | Fe2+ 与SCN-不能形成血红色的化合物 |
1.下列说法正确的是( )
| A. | 将SO2分别通入BaCl2、Ba(NO3)2溶液中,都会观察到有白色沉淀生成 | |
| B. | 检验某酸性溶液中Cl-、SO42-,选用试剂及顺序是过量的AgNO3溶液、Ba(NO3)2溶液 | |
| C. | 纯锌与稀硫酸反应产生氢气的速率较慢,加入少量硫酸铜固体后,反应速率会加快 | |
| D. | 对于任意化学平衡,只要增大反应物浓度,都会使反应物转化率增大 |
18.能用分液漏斗分离的混合物是( )
| A. | 液溴和四氯化碳 | B. | 乙二醇和水 | ||
| C. | NaCl溶液和高级脂肪酸 | D. | 饱和Na2CO3溶液和乙酸乙酯 |
19.下列相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| ① | 在两份同浓度同体积的H2O2溶液中,分别加2滴FeCl3溶液和2滴CuCl2溶液,前者放在热水中,后者放在冰水中.观察气泡快慢; | 验证温度对化学反应速率的影响. |
| ② | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| ③ | 在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率. | 比较同周期金属元素的金属性强弱. |
| ④ | 利用电解质溶液的导电性装置,检测AlCl3溶液的导电性 | 证明AlCl3是离子化合物 |
| A. | 仅① | B. | ①④ | C. | ②③ | D. | ③④ |
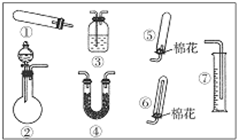 某同学用如图装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究.回答下列问题:
某同学用如图装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究.回答下列问题: