题目内容
【题目】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:______________;农业上用石膏降低其碱性的反应原理:__________。
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________(填“>”“<”或“=”)n。
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=__________。
(4)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(![]() )=c(Cl-),则溶液显________(填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=________。
)=c(Cl-),则溶液显________(填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=________。
【答案】Na2CO3+H2O![]() NaHCO3+NaOH Na2CO3+CaSO4=CaCO3+Na2SO4 < 1.0×10-8 mol·L-1 中
NaHCO3+NaOH Na2CO3+CaSO4=CaCO3+Na2SO4 < 1.0×10-8 mol·L-1 中 ![]()
【解析】
(1)碳酸钠在溶液中水解使溶液显碱性,导致盐碱地呈碱性,水解的化学方程式为Na2CO3+H2O ![]() NaHCO3+NaOH;向盐碱地中加入石膏(CaSO4),CaSO4和Na2CO3反应生成硫酸钠和碳酸钙,反应的化学方程式为:Na2CO3+CaSO4=CaCO3+Na2SO4,盐碱地中碳酸钠的浓度减小,使盐碱地中氢氧根浓度减小,碱性减弱,故答案为:Na2CO3+H2O
NaHCO3+NaOH;向盐碱地中加入石膏(CaSO4),CaSO4和Na2CO3反应生成硫酸钠和碳酸钙,反应的化学方程式为:Na2CO3+CaSO4=CaCO3+Na2SO4,盐碱地中碳酸钠的浓度减小,使盐碱地中氢氧根浓度减小,碱性减弱,故答案为:Na2CO3+H2O ![]() NaHCO3+NaOH;Na2CO3+CaSO4=CaCO3+Na2SO4;
NaHCO3+NaOH;Na2CO3+CaSO4=CaCO3+Na2SO4;
(2)氨水中存在电离平衡,稀释促进一水合氨的电离,使溶液中氢氧根的物质的量增加,而氢氧化钠在溶液中完全电离,不存在电离平衡,所以要使稀释的后的pH相等,氨水稀释的倍数大于氢氧化钠溶液,即m<n,故答案为:<;
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中醋酸的电离程度大于醋酸根的水解程度,醋酸电离出的氢离子抑制水的电离,则由水电离出来的c(OH-)=![]() mol/L=1×10-8mol/L,故答案为:1×10-8mol/L;
mol/L=1×10-8mol/L,故答案为:1×10-8mol/L;
(4)在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得n(NH3H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3H2O的电离常数Kb= 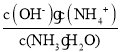 =
=![]() =
=![]() ,故答案为:中;
,故答案为:中;![]() 。
。

 阅读快车系列答案
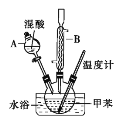
阅读快车系列答案【题目】邻硝基甲苯和对硝基甲苯能被用作爆炸品检测的示踪剂。某探究小组利用下图反应和装置制备一硝基甲苯。
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:
①按体积比1∶3配制浓硫酸与浓硝酸的混合物80mL;②在250mL的三颈烧瓶中加入30mL(26g)甲苯,按图所示装好药品和其他仪器;③向三颈烧瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);④控制温度约为50℃,反应大约10min,三颈烧瓶底有大量淡黄色油状液体出现;⑤分离出一硝基甲苯的总质量为27.20g。
请回答下列问题:
(1)使用仪器A前必须进行的操作是_______。
(2)该实验采用水浴加热,水浴加热的优点有:受热均匀、_______。
(3)配制混酸的方法是分别量取20mL浓硫酸和60mL浓硝酸,将浓_______倒入烧杯中,浓_______沿着烧杯内壁缓缓注入,并不断搅拌。
(4)控制温度约为50℃时,反应生成的产物一硝基甲苯是邻硝基甲苯和对硝基甲苯混合物,写出该反应生成对硝基甲苯的化学方程式_______。
(5)分离反应后产物的方案如下:

①操作1的名称为_______。
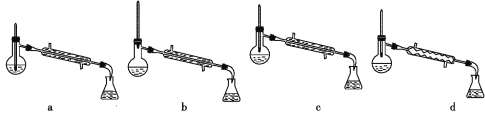
②操作2中,下列仪器选择及安装正确的是_______(填字母)。
(6)该实验中一硝基甲苯的产率为_______(保留两位有效数字)。