题目内容
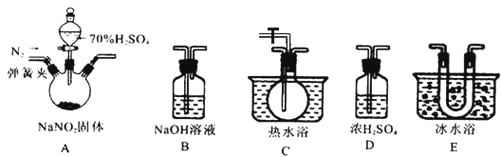
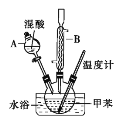
【题目】邻硝基甲苯和对硝基甲苯能被用作爆炸品检测的示踪剂。某探究小组利用下图反应和装置制备一硝基甲苯。
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:
①按体积比1∶3配制浓硫酸与浓硝酸的混合物80mL;②在250mL的三颈烧瓶中加入30mL(26g)甲苯,按图所示装好药品和其他仪器;③向三颈烧瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);④控制温度约为50℃,反应大约10min,三颈烧瓶底有大量淡黄色油状液体出现;⑤分离出一硝基甲苯的总质量为27.20g。
请回答下列问题:
(1)使用仪器A前必须进行的操作是_______。
(2)该实验采用水浴加热,水浴加热的优点有:受热均匀、_______。
(3)配制混酸的方法是分别量取20mL浓硫酸和60mL浓硝酸,将浓_______倒入烧杯中,浓_______沿着烧杯内壁缓缓注入,并不断搅拌。
(4)控制温度约为50℃时,反应生成的产物一硝基甲苯是邻硝基甲苯和对硝基甲苯混合物,写出该反应生成对硝基甲苯的化学方程式_______。
(5)分离反应后产物的方案如下:

①操作1的名称为_______。
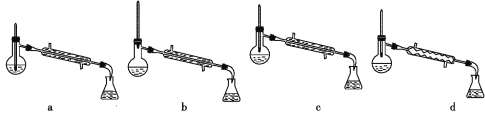
②操作2中,下列仪器选择及安装正确的是_______(填字母)。
(6)该实验中一硝基甲苯的产率为_______(保留两位有效数字)。
【答案】检查是否漏液 准确控制温度(其他合理答案也可) 硝酸 硫酸 ![]() +HNO3
+HNO3![]()
![]() +H2O 分液 b 70%
+H2O 分液 b 70%
【解析】
(1)仪器A是分液漏斗,使用前验漏;
(2)水浴加热的优点是避免了直接加热造成的受热不均与温度的不可控性,许多反应需要严格的温度控制,就需要水浴加热;
(3)类似浓硫酸的稀释,浓硫酸、浓硝酸混合应把浓硫酸倒入浓硝酸中;
(4)苯和浓硝酸、浓硫酸的混合物发生取代反应生成对硝基甲苯和水;
(5)①有机混合物和无机混合物是互不相溶的液体;
②蒸馏操作需要测蒸气的温度;
(6)根据甲苯是质量计算一硝基甲苯的理论质量,产率=实际产量÷理论产量×100%;
(1)仪器A是分液漏斗,使用前检查是否漏液;
(2)该实验采用水浴加热,水浴加热的优点有:受热均匀、准确控制温度;
(3)浓硫酸密度大于浓硝酸,应将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌,防止将浓硝酸加到浓硫酸中可能发生的液体飞溅;
(4)甲苯和浓硝酸、浓硫酸的混合物发生取代反应生成对硝基甲苯和水,反应的化学方程式是![]() +HNO3
+HNO3![]()
![]() +H2O;
+H2O;
(5)①有机混合物和无机混合物是互不相溶的液体,所以用分液法分离有机混合物和无机混合物;
②蒸馏操作需要测蒸气的温度,所以温度计液泡应在蒸馏烧瓶支管口处,选b;
(6)根据方程式![]() +HNO3
+HNO3![]()
![]() +H2O,26g甲苯理论上生成一硝基甲苯的质量是
+H2O,26g甲苯理论上生成一硝基甲苯的质量是![]() ,产率=实际产量÷理论产量×100%=27.20g÷38.7g×100%=70%。
,产率=实际产量÷理论产量×100%=27.20g÷38.7g×100%=70%。