题目内容
12.下列有关钢铁的腐蚀与防护的说法正确的是( )| A. | 钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+ | |
| B. | 钢铁发生析氧腐蚀的时候正极反应是2H2O+O2+e-═4OH- | |
| C. | 钢管与电源负极相连时,钢管可被保护 | |
| D. | 在入海口的钢铁闸门上装一定数量的铜块,可防止闸门被腐蚀 |
分析 A.钢铁发生析氢腐蚀时,负极上铁失电子生成亚铁离子;
B.钢铁发生析氢腐蚀时,正极上氢离子得电子生成氢气;
C.作电解池阴极的金属被保护;
D.作原电池正极或电解池阴极的金属被保护,作原电池负极或电解池阳极的金属加速被腐蚀.
解答 解:A.钢铁发生析氢腐蚀或吸氧腐蚀时,负极反应式都是Fe-2e-=Fe2+,故A错误;
B.钢铁发生吸氧腐蚀时,正极反应式为:2H2O+O2+4e-=4OH-,不管什么原电池反应,发生析氢腐蚀时正极反应式为2H++2e-=H2↑,故B正确;
C.电解池是“牺牲阳极的阴极保护法”,所以是保护阴极,阴极是连接电池负极的一极,则钢管与电源负极相连时,钢管可被保护,故C正确;
D.作原电池正极或电解池阴极的金属被保护,作原电池负极或电解池阳极的金属加速被腐蚀,Cu、Fe和电解质溶液构成原电池时,Fe易失电子作负极,加速被腐蚀,故D错误;
故选BC.
点评 本题考查金属腐蚀与防护,明确原电池和电解池原理是解本题关键,防止金属被腐蚀有物理方法和化学方法,会利用化学原理解释生活现象,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O+HA→CH3-CO-A.乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
| A. | 与HCl加成生成CH3COCl | B. | 与H2O加成生成CH3COOH | ||
| C. | 与CH3COOH加成生成CH3COOCOCH3 | D. | 与CH3OH加成生成CH3COCH2OH |
7.能与NaOH溶液反应放出气体,向反应后的溶液里通入足量CO2时能得到沉淀的是( )
| A. | Mg | B. | Al | C. | Si | D. | Cl2 |
17.下列物质中不容易分解的是( )
| A. | Fe(OH)3 | B. | NaOH | C. | HClO | D. | NaHCO3 |
4.根据你的实验观察和记录,下面关于Na2CO3和NaHCO3性质的叙述,正确的是( )
| A. | 受热时Na2CO3比NaHCO3稳定 | |
| B. | 同温同压下,在水中Na2CO3比NaHCO3溶解性小 | |
| C. | 物质的量相等的Na2CO3和NaHCO3分别溶于等体积的水后,Na2CO3水溶液的碱性较弱 | |
| D. | 质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,Na2CO3放出的CO2少 |
1.下列反应中,硫酸不作氧化剂的是( )
| A. | 2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2+SO2↑+2H2O | |
| B. | Ca3(PO4)2+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+Ca(H2PO4)2 | |
| C. | 2Al+3H2SO4═Al2(SO4)3+3H2↑ | |
| D. | 2KMnO4+5H2S+3H2SO4═K2SO4+2MnSO4+5S↓+8H2O |
2.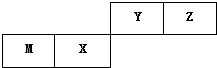 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )| A. | 原子半径Z<M | |
| B. | Y的最高价氧化物对应水化物的酸性比X的弱 | |
| C. | 非金属性:X>Z | |
| D. | M元素最高价氧化物对应水化物具有两性 |
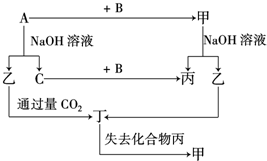 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图所示的转换关系,已知C为密度最小的气体,甲是电解质.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图所示的转换关系,已知C为密度最小的气体,甲是电解质. .
.