题目内容
2.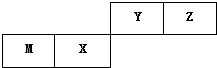 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )| A. | 原子半径Z<M | |
| B. | Y的最高价氧化物对应水化物的酸性比X的弱 | |
| C. | 非金属性:X>Z | |
| D. | M元素最高价氧化物对应水化物具有两性 |
分析 由四种短周期元素在周期表中的位置可知,Y、Z处于第二周期,M、X处于第三周期,其中只有M元素原子最外层电子数与电子层数相等,则M为Al,可推知X为Si、Y为N、Z为O.
A.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大;
B.非金属性越强,最高价氧化物对应水化物的酸性越强;
C.同周期随原子序数增大元素非金属性增强,同主族自上而下元素非金属性减弱;
D.氢氧化铝是两性氢氧化物.
解答 解:由四种短周期元素在周期表中的位置可知,Y、Z处于第二周期,M、X处于第三周期,其中只有M元素原子最外层电子数与电子层数相等,则M为Al,可推知X为Si、Y为N、Z为O,
A.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径Z<M,故A正确;
B.同周期随原子序数增大元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性X<Y,非金属性越强,最高价氧化物对应水化物的酸性越强,故B错误;
C.同周期随原子序数增大元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性:X<Z,故C错误;
D.氢氧化铝溶于强酸、强碱生成相应的盐与水,是两性氢氧化物,故D正确,
故选AD.
点评 本题考查元素周期表与元素周期表,侧重对元素周期律的考查,注意整体把握元素周期表的结构、理解元素周期律,难度不大.

练习册系列答案
相关题目
12.下列有关钢铁的腐蚀与防护的说法正确的是( )
| A. | 钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+ | |
| B. | 钢铁发生析氧腐蚀的时候正极反应是2H2O+O2+e-═4OH- | |
| C. | 钢管与电源负极相连时,钢管可被保护 | |
| D. | 在入海口的钢铁闸门上装一定数量的铜块,可防止闸门被腐蚀 |
13.下列反应里,有机物分子中断裂的共价键是π键的是( )
| A. | 甲烷与氯气发生取代反应 | B. | 乙烯与溴水发生加成反应 | ||
| C. | 氯气与氢气反应生成氯化氢 | D. | 乙醇与乙酸的酯化反应 |
10.两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法不正确的是( )
| A. | 若8>m>3,则X必定为主族元素 | |
| B. | 若a<b<m=n=4,则晶体类型相同时,其单质熔点:X>Y | |
| C. | 若Y的气态氢化物化学式为YHn,且b<4,则该氢化物为非极性分子 | |
| D. | 若a=b=3,8>m>n>b,则元素非金属性:X>Y |
17.下列物质的水溶液呈酸性的是( )
| A. | K2SO4 | B. | NaHSO4 | C. | Na2SiO3 | D. | NH3 |
14.下列现象或事实与对应的理论根据错误的是( )
| 选项 | 现象或事实 | 理论根据 |
| A | 稳定性:HF>HCl | 分子间的作用力大小 |
| B | 沸点:H2O>H2S | 氢键 |
| C | 碘单质在水溶液中溶解度很小,但在苯中溶解度很大 | 相似相溶原理 |
| D | 熔点:Al>Mg | 金属键 |
| A. | A | B. | B | C. | C | D. | D |
11.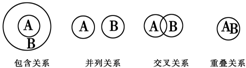 化学概念在逻辑上存在如下关系:对下列概念的说法正确的是( )
化学概念在逻辑上存在如下关系:对下列概念的说法正确的是( )
 化学概念在逻辑上存在如下关系:对下列概念的说法正确的是( )
化学概念在逻辑上存在如下关系:对下列概念的说法正确的是( )| A. | 化合物与电解质属于重叠关系 | B. | 化合物与碱性氧化物属于交叉关系 | ||
| C. | 溶液与胶体属于并列关系 | D. | 离子化合物和电解质属于交叉关系 |
4.室温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42-、S2O32- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+ | |
| C. | 在由水电离出的c(H+)=1×10-12mol/L的溶液:Fe3+、ClO-、Na+、SO42- | |
| D. | c(Fe2+)=0.1mol/L的溶液:H+、Al3+、NO3-、SCN- |