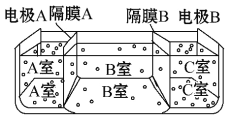
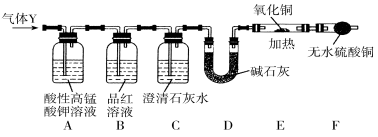
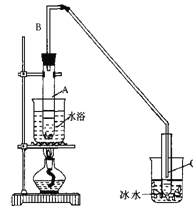
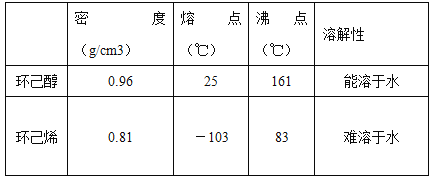
题目内容
【题目】常温下将0.04克氢氧化钠溶于水配制成100 mL溶液物质的量浓度为____mol/L; pH为______,要使它的pH降为11。(假设溶液混合体积等于稀释前两液体体积之和)若加入蒸馏水,应加________mL。若加入pH为10的NaOH溶液,应加______mL。若加入0.01 mol·L-1的盐酸,应加________mL(保留三位有效数字)。
【答案】0.01mol/l 12 900 1000 81.8
【解析】
试题分析:0.04克氢氧化钠的物质的量为![]() =0.001mol,溶于水配制成100 mL溶液物质的量浓度为
=0.001mol,溶于水配制成100 mL溶液物质的量浓度为![]() =0.01mol/L,pH=-lgc(H+)=-lg
=0.01mol/L,pH=-lgc(H+)=-lg![]() =-lg
=-lg![]() =12;
=12;
设加入蒸馏水的体积为x,pH=11,则c(OH-)=1×10-3mol/L,c(OH-)=![]() =1×10-3mol/L,解得x=0.9L=900mL,
=1×10-3mol/L,解得x=0.9L=900mL,
设加入pH为10的NaOH溶液的体积为y,c(OH-)=![]() =1×10-3mol/L,解得:y=1L=1000mL,
=1×10-3mol/L,解得:y=1L=1000mL,
设加入0.01 mol·L-1的盐酸的体积为z,c(OH-)=![]() =1×10-3mol/L,解得:z=0.0818L=81.8mL。
=1×10-3mol/L,解得:z=0.0818L=81.8mL。

练习册系列答案
相关题目