题目内容
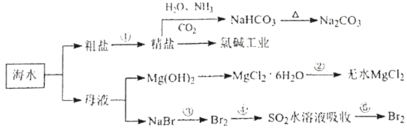
【题目】海水化学资源开发利用的部分过程如图所示,下列说法正确的是( )
A.用澄清的石灰水可鉴别NaHCO3和Na2CO3
B.从海水中得到粗盐主要是通过蒸发操作实现的
C.在步骤③,中可通入Cl2使溴离子被还原为Br2
D.在步骤④中,SO2水溶液吸收Br2后,溶液的pH增大
【答案】B
【解析】
海水蒸发溶剂得到粗盐和母液,粗盐通过精制得到精盐,电解饱和食盐水得到氯气、氢气和氢氧化钠,工业上制得饱和食盐水,依次通入氨气、二氧化碳反应生成碳酸氢钠和氯化铵,碳酸氢钠受热分解生成碳酸钠,母液加氢氧化钠反应生成氢氧化镁沉淀,氢氧化镁和酸反应生成氯化镁,制得氯化镁,母液通入氯气氧化溴离子为溴单质,被二氧化硫吸收后发生氧化还原反应生成溴化氢溶液,富集溴元素,通入氯气氧化溴化氢为溴单质得到溴,以此解答该题。
A. 在NaHCO3或Na2CO3中加入澄清的石灰水,现象均为产生白色沉淀,所以不能用澄清的石灰水鉴别NaHCO3和Na2CO3,A错误;
B. 氯化钠的溶解度随温度的变化不明显,故从海水中得到粗盐采用的是蒸发结晶的方法,B正确;
C. 步骤③中发生反应的化学方程式为:2NaBr+Cl2= Br2+2NaCl,Br的化合价由-1价升高为0价,溴离子被氧化为Br2,C错误;
D. 步骤④中SO2水溶液吸收Br2,发生反应的化学方程式为:SO2+Br2+2H2O=H2SO4+2HBr,溶液的酸性增强,pH减小,D错误;故答案为:B。

练习册系列答案
相关题目