题目内容
8.中国古代四大发明之一的黑火药,它的爆炸反应为:2KNO3+3C+S$\frac{\underline{\;点燃\;}}{\;}$A+N2↑+3CO2↑(已配平)①A是K2S.(写化学式)
②除S外,上列元素的电负性从大到小依次为O>N>C>K.
③在生成物中,A的晶体类型为离子晶体
④已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为1:1.
分析 ①由质量守恒定律可知,反应前后原子个数不变;
②同周期自左而右电负性增大,金属性越强电负性越小,据此解答;
③由原子守恒可知,物质A为K2S,属于离子晶体;含极性共价键的分子为CO2,分子中C原子形成2个C=O键,不含孤对电子,杂化轨道数目为2;
④CN-与N2结构相似,C原子与N原子之间形成三键,则HCN分子结构式为H-C≡N,三键中含有1个σ键、2个π键,单键属于σ键.
解答 解:①由化学方程式为2KNO3+3C+S$\frac{\underline{\;点燃\;}}{\;}$A+N2↑+3CO2↑,根据质量守恒定律可知,反应前后元素种类、原子个数相等,N、O、C的原子个数前后相等,而反应物中有S、K元素,生成物中应一定有S、K元素,则X中含有S、K元素,反应前共1个S原子,共2个K原子,则Y中共1个S原子,共2个K原子,又X的化学计量数为1,则A的化学式为K2S,故答案为:K2S;
②同周期自左而右电负性增大,金属性越强电负性越小,故电负性O>N>C>K,
故答案为:O>N>C>K;
③由原子守恒可知,物质A为K2S,属于离子晶体,故答案为:离子晶体;
④CN-与N2结构相似,C原子与N原子之间形成三键,则HCN分子结构式为H-C≡N,三键中含有1个σ键、2个π键,单键属于σ键,故HCN分子中σ键与π键数目之比为1:1,故答案为:1:1.
点评 本题考查了电负性、晶体类型、等电子体等知识,题目难度不大,注意对基础知识的理解掌握,注意④CN-与N2为等电子体,推算HCN分子中σ键与π键数目之比为易错点.

练习册系列答案
相关题目
18.某种发动机燃料由A、B两种物质混合而成,A、B两种物质含有C、H、O三种元素中的两种或三种.已知常温下,A、B及CO、H2的燃烧热如下:
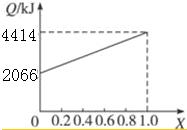
A、B按不同比例混合的燃料91.2 g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如上图.
(1)A、B的相对分子质量为A32,B114.
(2)等物质的量的A、B混合的燃料73 g,在160L O2中完全燃烧,反应后气体通过浓硫酸后,得到104L气体,通过碱石灰吸收后剩余3.2 L(气体体积均在标准状况下测定).由此可推得混合物中N(C):N(H):N(O)=9:22:1,A分子式为CH4O,B分子式为C8H18.
(3)1 mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980 kJ,则反应中生成CO0.5
mol.
| 物质 | A | B | CO | H2 |
| 燃烧热/kJ•mol-1 | 725 | 5 518 | 283 | 286 |

A、B按不同比例混合的燃料91.2 g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如上图.
(1)A、B的相对分子质量为A32,B114.
(2)等物质的量的A、B混合的燃料73 g,在160L O2中完全燃烧,反应后气体通过浓硫酸后,得到104L气体,通过碱石灰吸收后剩余3.2 L(气体体积均在标准状况下测定).由此可推得混合物中N(C):N(H):N(O)=9:22:1,A分子式为CH4O,B分子式为C8H18.
(3)1 mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980 kJ,则反应中生成CO0.5
mol.
19.某条件下,恒容密闭容器中发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应),下列说法正确的是( )
| A. | 用高效催化剂,可提高CO2的利用率 | |
| B. | 单位时间内消耗CO2和H2的物质的量比为1:3时,反应达到平衡 | |
| C. | 及时分离出CH3OH和H2O可提高CO2和H2的利用率 | |
| D. | 升高温度可使该反应向正反应方向移动 |
16.下列物质属于苯的同系物是( )
| A. | 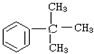 | B. |  | C. | 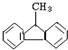 | D. | 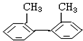 |
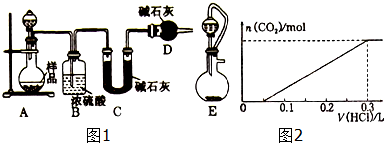
3.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的化学方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,该现象不能(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是过量的Cl2也可以将I-氧化为I2.
(5)装置F的作用是吸收多余的氯气,防止污染大气,其烧杯中的溶液 不能选用下列中的b(填字母编号).
a.饱和NaOH溶液
b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液
d.饱和Na2CO3溶液.

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的化学方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)装置F的作用是吸收多余的氯气,防止污染大气,其烧杯中的溶液 不能选用下列中的b(填字母编号).
a.饱和NaOH溶液
b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液
d.饱和Na2CO3溶液.
20.下列描述中正确的是( )
| A. | 氮原子的价电子排布图: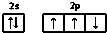 | |
| B. | 2p和3p轨道形状均为哑铃形,能量也相等 | |
| C. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| D. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 |
17.下列性质能肯定该物质为离子化合物的是( )
| A. | 第ⅠA族与第ⅦA族元素形成的化合物 | B. | 溶于水中能导电的化合物 | ||
| C. | 在熔化状态下能导电的化合物 | D. | 熔点高的化合物 |