��Ŀ����
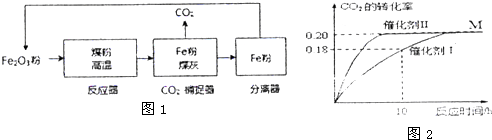
17����������11����ѧ��ѧ���������ʣ���һ�������¿���ʵ����ͼ��ʾ��ת����ϵ��ͼ��ijЩ��Ӧ����������Ѿ���ȥ��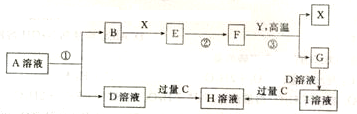
��֪��AΪ����Ԫ����ɵĻ��������ɫ��Ӧ����ɫ�ܲ����۲쵽Ϊ��ɫ��BΪ���ʣ���һ���ж����壻��Ӧ�ٵ��������ö��Ե缫��⣻��Ӧ�ڵ������ǽ�E��ˮ��Һ�������ɡ����գ�YΪ����������F�н���Ԫ�أ�+3�ۣ��������Ϊ70%��CΪ����22���ӵ�������ش��������⣺
��1��D�ĵ���ʽΪ
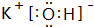 ��H�Ļ�ѧʽΪKHCO3��
��H�Ļ�ѧʽΪKHCO3����2����Ӧ�۵Ļ�ѧ����ʽΪ2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+Al2O3������Cͨ��I��Һ�з�����Ӧ�����ӷ���ʽΪCO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
��3��ָ��G��һ����;���ͻ���ϣ�
��4����һ������Bͨ�˵�����l mol XBr2����Һ�У�����$\frac{1}{3}$��Brһ����������ͨ���B�ڱ�״���µ����Ϊ18.7L������һλС������
��5����ͬѧ˵���������������������x����������Һ�������ɺ�õ��Ĺ��������E�������ɺ�õ��Ĺ�������ͬ�ġ������˵���Ƿ���ȷ������ȷ�����ȷ������ȷ������������������ˮ�����ɵIJ��ӷ�����--���ᣬ���������������Ӧ������������������������Һ�������ɵõ��Ǵ��ᾧˮ�����������壬���Ȼ���ˮ�����ɻӷ�����--���ᣬʹ�Ȼ�����ˮ�⳹���е��ף����Ȼ�����Һ�������ɵõ���ˮ����������
���� AΪ����Ԫ����ɵĻ��������ɫ��Ӧ����ɫ�ܲ����۲쵽Ϊ��ɫ����A����KԪ�أ��ö��Ե缫���A����Һ�õ�BΪ������һ���ж����壬��AΪKCl��BΪCl2����ҺDΪKOH��CΪ����22���ӵ����������KOH��Һ��Ӧ����CΪCO2��HΪKHCO3����Ӧ�ڵ������ǽ�E��ˮ��Һ�������ɡ����գ�F�н���Ԫ�أ�+3�ۣ��������Ϊ70%������֪XΪFe��FΪFe2O3��YΪ������������Ӧ��Ϊ���ȷ�Ӧ��YΪAl��GΪAl2O3��IΪNaAlO2���ݴ˽��
��� �⣺AΪ����Ԫ����ɵĻ��������ɫ��Ӧ����ɫ�ܲ����۲쵽Ϊ��ɫ����A����KԪ�أ��ö��Ե缫���A����Һ�õ�BΪ������һ���ж����壬��AΪKCl��BΪCl2����ҺDΪKOH��CΪ����22���ӵ����������KOH��Һ��Ӧ����CΪCO2��HΪKHCO3����Ӧ�ڵ������ǽ�E��ˮ��Һ�������ɡ����գ�F�н���Ԫ�أ�+3�ۣ��������Ϊ70%������֪XΪFe��FΪFe2O3��YΪ������������Ӧ��Ϊ���ȷ�Ӧ��YΪAl��GΪAl2O3��IΪNaAlO2��
��1��DΪKOH������ʽΪ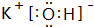 ��H�Ļ�ѧʽΪKHCO3��
��H�Ļ�ѧʽΪKHCO3��
�ʴ�Ϊ��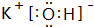 ��KHCO3��
��KHCO3��
��2����Ӧ�۵Ļ�ѧ����ʽΪ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+Al2O3������Cͨ��I��Һ�з�����Ӧ�����ӷ���ʽΪ��CO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+Al2O3��CO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
��3��GΪAl2O3������ұ���������������ͻ���ϣ�
�ʴ�Ϊ���ͻ���ϣ�
��4����һ����������ͨ�˵�����l mol FeBr2����Һ�У�����$\frac{1}{3}$��Br-��������˵������������ȫ�����������ݵ���ת���غ㣬��֪ͨ������Ϊ$\frac{1mol����3-2��+2mol��\frac{1}{3}��1}{2}$=$\frac{5}{6}$mol��������ͨ���������Ϊ$\frac{5}{6}$mol��22.4L/mol=18.7L��
�ʴ�Ϊ��18.7��
��5��������ˮ�����ɵIJ��ӷ�����--���ᣬ���������������Ӧ������������������������Һ�������ɵõ��Ǵ��ᾧˮ�����������壬���Ȼ���ˮ�����ɻӷ�����--���ᣬʹ�Ȼ�����ˮ�⳹���е��ף����Ȼ�����Һ�������ɵõ���ˮ����������
�ʴ�Ϊ������ȷ��������ˮ�����ɵIJ��ӷ�����--���ᣬ���������������Ӧ������������������������Һ�������ɵõ��Ǵ��ᾧˮ�����������壬���Ȼ���ˮ�����ɻӷ�����--���ᣬʹ�Ȼ�����ˮ�⳹���е��ף����Ȼ�����Һ�������ɵõ���ˮ����������
���� ���⿼�������ƶϣ���Ҫѧ����������Ԫ�ػ��������ʣ��漰����ʽ������ʽ��д��������ԭ��Ӧ���㡢����ˮ��ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�

 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д� ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д����Ȼ��� ��̼���� ���������� �ܹ����ƣ�
| A�� | ���٢� | B�� | ���ڢ� | C�� | ���٢ۢ� | D�� | ���٢ڢ� |
| A�� | ��ǦԪ��ԭ�ӵ�����������Ϊ6 | B�� | �䳣����̬Ϊ+2��+3��+4 | ||
| C�� | ���Ľ����Ա�Ǧǿ | D�� | ����ԭ�Ӱ뾶��ǦС? |
| A�� |  ���� | B�� | 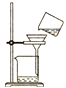 ���� | C�� |  ��Һ | D�� |  ���� |
| A�� | ��FeBr2��Һ��ͨ������Cl2��Cl2+2Br-�T2Cl-+Br2 | |
| B�� | ��ȥMgCl2��Һ��������FeCl3��3Mg+2Fe3+�T2Fe+3Mg2+ | |
| C�� | ���а�ˮ��BaCl2��Һ��ͨ��SO2��SO2+2NH3•H2O+Ba2+�TBaSO3��+2NH4++H2O | |
| D�� | ������������̼ͨ���Ȼ�����Һ�У�Ca2++CO2+H2O�TCaCO3+2H+ |
| A�� | 1 mol ������6 NA��C-H�� | |
| B�� | ���³�ѹ�£�22.4 L H2O����3NA��ԭ�� | |
| C�� | 1L 0.1 mol•L-1NaHCO3��Һ�к���0.1NA��HCO3- | |
| D�� | 23g Na������H2O��Ӧ��ȫ��ת��2NA������ |
��1����������������Ӧ����1molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-241.8kJ/mol����1gˮ����ת����Һ̬ˮ����2.444kJ����Ӧ2H2��g��+O2��g���T2H2O��l���ġ�H=-571.6kJ/mol��������ȼ����Ϊ285.8kJ/mol��
��2������̬��̬ԭ���γ�1mol��ѧ���ͷŵ���������м��ܣ��ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣��ڻ�ѧ��Ӧ�����У��ƻ��ɻ�ѧ����Ҫ�����������γ��»�ѧ���ֻ��ͷ�������
| ��ѧ�� | H-H | N-H | N��N |
| ����/kJ•mol-1 | 436 | 391 | 945 |
��3�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ���ʱ�������㣮
��֪��C��s��ʯī��+O2��g���TCO2��g����H1=-393.5kJ•mol-1
2H2��g��+O2��g���T2H2O��l����H2=-571.6kJ•mol-1
2C2H2��g��+5O2��g���T4CO2��g��+2H2O��l����H3=-2 599kJ•mol-1
���ݸ�˹���ɣ�����298Kʱ��C��s��ʯī����H2��g������1mol C2H2��g����Ӧ���ʱ䣨�г��ļ���ʽ������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3=+226.7kJ•mol-1��
| A�� | ����ϩ�����к�̼̼˫�� | B�� | ��֬��������Ӧ���ڼӳɷ�Ӧ | ||
| C�� | ������3��ͬ���칹�� | D�� | �Ե���Ϊԭ�Ͽ����Ʊ��Ҵ� |