题目内容
8.某化学小组对以下四种物质的水溶液加热蒸干并灼热,最终不能得到该物质固体的是( )①氯化铁 ②碳酸钠 ③硫酸亚铁 ④硅酸钠.
| A. | 仅①③ | B. | 仅②④ | C. | 仅①③④ | D. | 仅①②③ |
分析 加热蒸干并灼烧的过程中,要注意考虑盐的水解平衡的移动、物质的氧化、物质的分解等情况,氯化铁易水解,硫酸亚铁易被氧化等.
解答 解:①FeCl3因为能水解生成Fe(OH)3,灼烧得Fe2O3,溶液加热蒸干并灼热不能得到原物质,故正确;
②碳酸钠在溶液在加热时水解得到碳酸氢钠与氢氧化钠,但氢氧化钠难挥发,最后得到的固体为Na2CO3,故错误;
③硫酸亚铁易被氧化为硫酸铁,加热蒸干得到的是硫酸铁,溶液加热蒸干并灼热不能得到原物质,故正确;
④硅酸钠中硅酸根离子水解得到硅酸,硅酸受热分解为二氧化硅,溶液加热蒸干并灼热不能得到原物质,故正确;
故选C.
点评 本题综合考查物质的性质,侧重于水解、分解等知识,题目难度不大,注意相关物质的性质的掌握.

练习册系列答案
相关题目
15.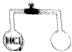 如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
 如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )| A. | O3、N2 | B. | CH4、NH3 | C. | N2、O2 | D. | CO、CO2 |
19.下列说法正确的是( )
| A. | 所有的化学反应都有能量变化 | |
| B. | 需要加热的反应一定是吸热反应 | |
| C. | 所有的放热反应都可以在常温常压下自发进行 | |
| D. | 核能作为一种反应热,是理想的新能源 |
16.由FeO、Fe2O3和Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21:8,则这种混合物中FeO、Fe2O3和Fe3O4的物质的量之比是( )
| A. | 1:1:1 | B. | 2:1:1 | C. | 1:2:1 | D. | 1:1:3 |
3.同温同压下,下列各热化学方程式中热量数值最小的是( )
| A. | 2A(l)+B(l)═2C(g);△H=+Q1 | B. | 2A(g)+B(g)═2C(g);△H=+Q2 | ||
| C. | 2A(g)+B(g)═2C(l);△H=+Q3 | D. | 2A(l)+B(l)═2C(l);△H=+Q4 |
13.汽车尾气中二氧化硫、氮氧化物和可吸入颗粒物是雾霾主要组成.某课题组用汽车尾气为原料探究二氧化硫、氮氧化物的化学性质.
I.汽车尾气(含有烃类、CO、SO2与NO等物质),冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化.写出一氧化碳与一氧化氮反应的化学方程式:2CO+2NO?2CO2+N2
Ⅱ.课题组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:
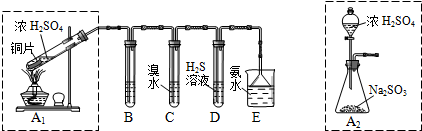
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液;
C中反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+.
(2)为了实现绿色环保的目标,制取SO2装置最好选择A2.(A1或A2装置)用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为NH3•H2O+SO2=NH4++HSO3-.
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/LHNO3、1mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
I.汽车尾气(含有烃类、CO、SO2与NO等物质),冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化.写出一氧化碳与一氧化氮反应的化学方程式:2CO+2NO?2CO2+N2
Ⅱ.课题组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液;
C中反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+.
(2)为了实现绿色环保的目标,制取SO2装置最好选择A2.(A1或A2装置)用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为NH3•H2O+SO2=NH4++HSO3-.
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/LHNO3、1mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体滴入1滴品红,再滴入过量2 mol/L盐酸,振荡 用试管取适量滤液,向其中滴入过量l mol/LBa(OH)2溶液(或1滴品红,再滴入2-3滴2 mol/L盐酸),振荡. 步骤3: | 若品红褪色(或有气泡)则存在SO32- 若出现白色沉淀(或品红褪色或有气泡),则存在HSO3- |
20.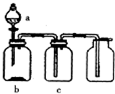 使用下表提供的试剂,利用如图所示的装置,能达到实验目的是( )
使用下表提供的试剂,利用如图所示的装置,能达到实验目的是( )
 使用下表提供的试剂,利用如图所示的装置,能达到实验目的是( )
使用下表提供的试剂,利用如图所示的装置,能达到实验目的是( )| 选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 |
| A | 稀盐酸 | 铁粉 | H2O | 制备并收集H2 |
| B | 稀硫酸 | Na2SO3粉末 | 浓硫酸 | 制备并收集干燥的SO2 |
| C | 浓盐酸 | KmnO4粉末 | NaOH溶液 | 制备并收集Cl2 |
| D | 浓氨水 | 生石灰 | 碱石灰 | 制备并收集干燥的NH3 |
| A. | A | B. | B | C. | C | D. | D |
17.工业上常用水杨酸与乙酸酐反应制取解热镇痛药阿司匹林(乙酰水杨酸).
【反应原理】
如图1
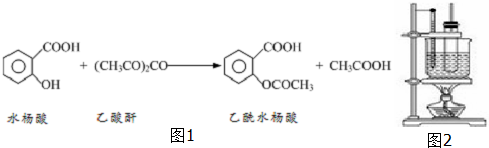
【物质性质】
【实验流程】
(1)物质制备:向大试管中依次加入2g水杨酸、5mL乙酸酐(密度为1.08g/mL)、5滴浓硫酸,振荡大试管至水杨酸全部溶解,将其放入盛有热水烧杯中,固定在铁架台上,在85℃~90℃条件下加热5~10min.装置如图2:
(2)产品结晶:取下大试管,置于冷水中冷却10min.待晶体完全析出,…抽滤,再洗涤晶体,抽干.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂NaHCO3并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸1.8g.
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色.
【问题讨论】
(1)写出水杨酸与碳酸氢钠溶液反应的化学反应方程式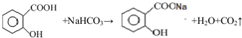 .
.
(2)写出水杨酸与足量碳酸钠溶液反应后含苯环的生成物的结构简式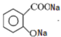 .
.
(3)流程(1)装置图中长导管的作用冷凝回流和平衡压强.
(4)控制反应温度85℃~90℃的原因既保持有较高的反应速率又减少物质的挥发.
(5)流程(2)中证明晶体洗涤干净的操作方法:取最后一次洗涤滤液少许于试管中,滴加少量氯化钡,再滴加稀盐酸,若无沉淀出现则洗涤干净,反之则未洗涤干净
(6)流程(4)中溶液显紫色,可能的原因是产品中仍然可能有水杨酸.
(7)1mol乙酰水杨酸与氢氧化钠溶液反应可能,最多消耗3mol NaOH.
(8)实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
【反应原理】
如图1

【物质性质】
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 乙酸酐 | 139 | 在水中逐渐分解 | 略 |
| 乙酰水杨酸 | 略 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | 略 |
| 乙酸 | 117.9 | 略 | 略 |
(1)物质制备:向大试管中依次加入2g水杨酸、5mL乙酸酐(密度为1.08g/mL)、5滴浓硫酸,振荡大试管至水杨酸全部溶解,将其放入盛有热水烧杯中,固定在铁架台上,在85℃~90℃条件下加热5~10min.装置如图2:
(2)产品结晶:取下大试管,置于冷水中冷却10min.待晶体完全析出,…抽滤,再洗涤晶体,抽干.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂NaHCO3并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸1.8g.
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色.
【问题讨论】
(1)写出水杨酸与碳酸氢钠溶液反应的化学反应方程式
 .
.(2)写出水杨酸与足量碳酸钠溶液反应后含苯环的生成物的结构简式
 .
.(3)流程(1)装置图中长导管的作用冷凝回流和平衡压强.
(4)控制反应温度85℃~90℃的原因既保持有较高的反应速率又减少物质的挥发.
(5)流程(2)中证明晶体洗涤干净的操作方法:取最后一次洗涤滤液少许于试管中,滴加少量氯化钡,再滴加稀盐酸,若无沉淀出现则洗涤干净,反之则未洗涤干净
(6)流程(4)中溶液显紫色,可能的原因是产品中仍然可能有水杨酸.
(7)1mol乙酰水杨酸与氢氧化钠溶液反应可能,最多消耗3mol NaOH.
(8)实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
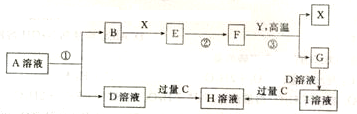
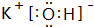 ,H的化学式为KHCO3;
,H的化学式为KHCO3;