题目内容
【题目】常温下,向20mL0.1molL-1Na2X溶液中缓慢滴加0.1molL-1盐酸溶液(不逸出H2X),溶液pH与溶液中lg![]() 之间关系如图所示。下列说法错误的是( )
之间关系如图所示。下列说法错误的是( )

A.M点:c(X2-)>c(HX-)>c(OH-)>c(H+)
B.常温下,0.1molNa2X和1molNaHX同时溶于水得到溶液pH=5.2
C.N点:c(Na+)<3c(X2-)+c(Cl-)
D.常温下,X2-第一步水解常数Kh1的数量级为10-8
【答案】B
【解析】
A.M点对应的溶液中,c(X2-)=10c(HX-),pH>7,呈碱性,c(OH- )>c(H+ ),溶液中离子浓度大小排序为c(X2-)>c(HX-)>c(OH- )>c(H+ ),A项正确;
B.1 mol NaHX和0.1 mol Na2X投人水中,NaHX电离大于Na2X水解,故溶液中lg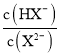 <1,pH>5.2,B项错误;
<1,pH>5.2,B项错误;
C.N点对应的溶液中电荷守恒式为c(Na+)+c(H+)=c(OH-)+c(HX-)+2c(X2-)+c(C1-),c(H+)>c(OH-),c(HX-)=c(X2-),整理得:c(Na+)<3c(X2-)+c(C1-),C项正确;
D.常温下,X2-+H2OHX-+OH-,选择N点对应的数据计算,Kb1=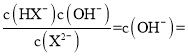 1×10-7.8=10-8×100.2,1<100.2<10,数量级为10-8,故D正确;
1×10-7.8=10-8×100.2,1<100.2<10,数量级为10-8,故D正确;
答案选B。

【题目】合成气(CO+H2)广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气。
(1)已知标况下,5.6LCH4与水蒸气完全反应时吸收51.5KJ的热量,请写出该反应的热化学方程式____;
(2)在150℃时2L的密闭容器中,将2 mol CH4和2 mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=____。
②在该温度下,计算该反应的平衡常数K=____。
③下列选项中能表示该反应已达到平衡状态的是____
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C (CH4) = C (CO)
(3)合成气中的氢气也用于合成氨气:N2 + 3H2![]() 2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
容 器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2的 体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | ν甲 | P甲 |
乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | ν乙 | P乙 |
丙 | 2L | 2molN2+6molH2 | n2 mol | span>φ丙 | ν丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.ν乙>ν丙>ν甲 D.P乙>P甲=P丙
(4)合成气制甲醚的反应方程式为2CO(g) + 4H2(g)![]() CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。
CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。

① 290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是____;
② b____0,(填“>”或“<”或“=”)理由是____。