题目内容
19.常温下,氯气是无色、有刺激性气味的气体,它的水溶液叫做氯水,其中含有次氯酸,所以它有强氧化作用.分析 氯气是无色、有刺激性气味的气体,它的水溶液叫做氯水,氯气与水反应生成氯化氢和次氯酸,含有次氯酸.
解答 解:常温下,氯气是无色、有刺激性气味的气体,它的水溶液叫做氯水,氯气与水反应生成氯化氢和次氯酸,其中含有次氯酸,次氯酸有强氧化作用,
故答案为:无;刺激性;氯水;次氯酸;强氧化.
点评 本题考查氯气的物理性质,难度不大,注意氯水的成分,学习中注意相关基础知识的积累.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
9.2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖.钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HCl.下列说法正确的是( )
| A. | 题述反应条件下还原性:CO>Pd | |
| B. | 题述反应中PdCl2被氧化 | |
| C. | 生成22.4 L CO2时,转移的电子为2 mo1 | |
| D. | CO气体只有在高温下才能表现还原性 |
10. 在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
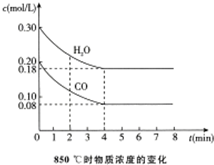
(1)850℃时,通入一定量的CO和H2O,CO和H2O浓度变化如图.
①0~4min的平均反应速率v(CO)=0.03mol/(L•min).
②850℃时,该反应的平衡常数K=1.
t1℃时物质浓度(mol/L)的变化
(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度数据如上表.
①上述两个温度下进行的反应,先达到化学平衡状态的温度是t1℃.
②c1>(填“>”“<”或“=”)0.08mol/L.
③反应在4min~5min之间时,若平衡逆向移动,可能的原因是d,表中5min~6min之间数值发生变化,可能的原因是a.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0(1)850℃时,通入一定量的CO和H2O,CO和H2O浓度变化如图.
①0~4min的平均反应速率v(CO)=0.03mol/(L•min).
②850℃时,该反应的平衡常数K=1.
t1℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①上述两个温度下进行的反应,先达到化学平衡状态的温度是t1℃.
②c1>(填“>”“<”或“=”)0.08mol/L.
③反应在4min~5min之间时,若平衡逆向移动,可能的原因是d,表中5min~6min之间数值发生变化,可能的原因是a.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
14.氯水的pH( )
| A. | 小于7 | B. | 等于7 | C. | 大于7 |
4.下列各反应中,属于原电池反应的是( )
| A. | 氧化铝膜别破坏后,金属铝被迅速氧化 | |
| B. | 白铁镀锌层破坏后,还能阻止铁被氧化 | |
| C. | 红热的铁与水接触表面上形成蓝黑色的保护层 | |
| D. | 铁与稀硫酸反应时,加入少量CuSO4溶液可使反应加快 |
11.下列各图象中指定时刻(t1)或指定温度(T1)时,表示可逆反应以达到平衡的是( )
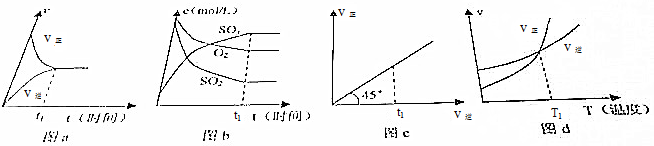

| A. | 只有图a和图b | B. | 只有图a和图d | ||
| C. | 只有图a、图b和图d | D. | 图a、图b、图c和图d都是 |
4.下列相关反应 的离子方程式或化学方程式书写正确的是( )
| A. | CuSO4溶液呈酸性的原因:Cu2++2H2O═Cu(OH)2↓+2H+ | |
| B. | 向NH4HCO3溶液中加过量石灰水并加热:${NH}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | Fe(OH)2溶于氨碘酸中:Fe(OH)3+3H+═Fe3++3H2O | |
| D. | 氧化亚铜和稀硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O |