题目内容
4.化合物D是硅橡胶的稳定剂,其合成路线如下图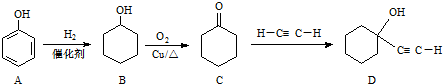
(1)B的分子式为C6H12O; C中官能团名称羰基.
(2)C→D的反应类型为加成反应.
(3)B→C的化学方程式为
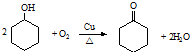 .
.(4)化合物D可能具有的性质有acd(选填序号).
a.加成反应 b.与FeCl3溶液发生显色反应c.消去反应 d.酯化反应
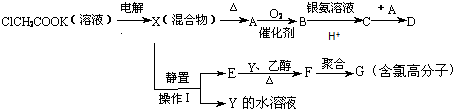
(5)化合物B经3步反应可制备
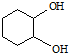 ,反应类型依次是c(选填序号).
,反应类型依次是c(选填序号).a.加成、取代、消去 b.取代、消去、加成 c.消去、加成、取代.
分析 (1)根据B和C的结构简式可判断;
(2)C→D的反应中,C中的碳氧双键与乙炔中的碳氢键加成得到D;
(3)B中的羟基被氧化成羰基得到C;
(4)化合物D中有羟基和碳碳参键;
(5)B经过消去生成碳碳双键,再与卤素单质加成,再水解可制得 ;
;
解答 解:(1)根据B和C的结构简式可知,B的分子式为C6H12O,C中含有的官能团为羰基,
故答案为:C6H12O;羰基;
(2)C→D的反应中,C中的碳氧双键与乙炔中的碳氢键加成得到D,
故答案为:加成反应;
(3)B中的羟基被氧化成羰基得到C,所以反应的化学方程式为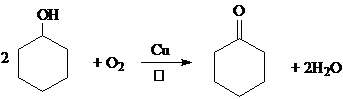
故答案为: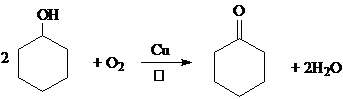
(4)化合物D中有醇羟基和碳碳参键,所以不能与FeCl3溶液发生显色反应,能发生加成反应、消去反应、酯化反应,故acd正确,
故答案为:acd;
(5)B经过消去生成碳碳双键,再与卤素单质加成,再水解可制得 ,所以反应类型依次是消去、加成、取代,
,所以反应类型依次是消去、加成、取代,
故答案为:c.
点评 本题考查有机物推断与合成,答题时要熟练掌握官能团的性质与转化,较好地考查学生自学能力、分析推理能力,难度不大.

练习册系列答案
相关题目
14.下列离子方程式书写正确是( )
| A. | 氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | |
| B. | 将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-=2Fe2++S↓ | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
15. 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 | |
| B. | ⑤的三种核素的化学性质不相同 | |
| C. | ⑥、⑧、⑨对应单核离子的半径依次增大 | |
| D. | ⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 |
12.下列变化属于化学变化的是( )
| A. | 碘的升华 | B. | 碘化银用于人工降雨 | ||
| C. | 液溴的气化 | D. | 漂白粉久置失效 |
19.下列关于化学反应中的能量变化的表述正确的是( )
| A. | 加热才能发生的反应一定是吸热反应 | |
| B. | 断开化学键的过程会吸收能量 | |
| C. | 化学能不仅可以与热能相互转化,还可以与电能相互转化 | |
| D. | 燃烧可能为吸热反应 |
9.下列叙述错误的是( )
| A. | 烷烃的沸点随碳原子数增加而逐渐升高 | |
| B. | 任何烷烃分子中碳氢原子个数比都是相同的 | |
| C. | 丙烷与Cl2发生取代反应后生成的一氯代物不只是一种 | |
| D. | 正丁烷的熔点、沸点比异丁烷的高 |
16.可以证明某化合物一定含有离子键的性质是( )
| A. | 熔融状态能导电 | B. | 具有较高的熔点 | C. | 可溶于水 | D. | 溶于水能导电 |
16.下列说法错误的是( )
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 在常温常压下,C4H10是气体 |
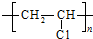 .
. .
.