题目内容
5.按要求写出下列反应的化学方程式或离子方程式:(1)用氢氧化钠除去氧化镁中的氧化铝(离子方程式):Al2O3+20H-+3H2O=2[Al(OH)]-.
(2)氢氟酸雕刻玻璃(化学方程式):SiO2+HF=SiF4↑+2H2O.
(3)向氯化铝中滴加氢氧化钠至过量(离子方程式):Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=[Al(OH)4]-.
分析 (1)氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水;
(2)氢氟酸能够与玻璃中的二氧化硅反应生成四氟化硅和水;
(3)向氯化铝中滴加氢氧化钠,开始氢氧化钠较少,反应产生氢氧化铝,此后过量的氢氧化钠将氢氧化铝溶解,生成偏铝酸钠和水.
解答 解:(1)氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O,离子方程式为:Al2O3+20H-+3H2O=2[Al(OH)]-,
故答案为:Al2O3+20H-+3H2O=2[Al(OH)]-;
(2)氢氟酸与二氧化硅反应的化学方程式为:SiO2+4HF═SiF4↑+2H2O,所以用氢氟酸能够雕刻玻璃,故答案为:SiO2+4HF═SiF4↑+2H2O;
(3)向氯化铝中滴加氢氧化钠,开始氢氧化钠较少,反应产生氢氧化铝,Al3++3OH-=Al(OH)3↓,过量的氢氧化钠将氢氧化铝溶解,生成偏铝酸钠和水:Al(OH)3+OH-=[Al(OH)4]-,故答案为:Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=[Al(OH)4]-.
点评 本题考查了离子方程式、化学方程式的书写方法和注意问题,难溶物、弱电解质、物质性质的分析判断是解题关键.题目较简单.

练习册系列答案
相关题目
15.含有非极性键的共价化合物是( )
| A. | Na2O2 | B. | H2O2 | C. | H2 | D. | HCl |
16.有关化学用语正确的是( )
| A. | 过氧化钠的电子式: | B. | 乙醇的分子式C2H5OH | ||
| C. | 硫离子的结构示意图: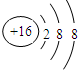 | D. | 乙酸的结构简式:C2H4O2 |
13.一定质量的下列各组物质的混合物,不管两者以何种质量比混合,充分燃烧后所生成的H2O的质量都相等,该混合物可能是( )
| A. | 乙醇和乙烯 | B. | 甲醛和葡萄糖 | C. | 乙烯和乙酸乙酯 | D. | 丙烷和乙醛 |
10.(1)A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如表所示:
根据上述信息,写出B的基态原子核外电子排布式1s22s22p63s2,预测A和氯元素形成的简单分子空间构型为直线型.
(2)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入AgNO3溶液时,无明显现象,往其溶液中加BaCl2溶液时若,产生白色沉淀,则该配合物的化学式为[Co(Br)(NH3)5]SO4,中心离子的配位数为6.
(3)参考下表中的物质熔点回答下列问题
根据上表数据解释钠的卤化物及碱金属的氯化物的熔点变化规律随阴阳离子的半径增大,熔降低点.
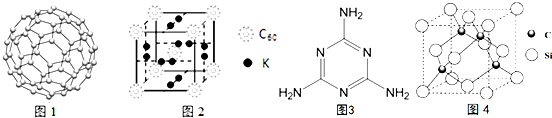
(4)C60可用作储氢材料.C60的结构如图1.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确不正确,并阐述理由C60是分子晶体,熔化时不需破坏化学键.科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体,该物质的K原子和C60分子的个数比为3:1.
 σ
σ
(5)三聚氰胺分子的结构简式如图3,则其中氮原子轨道杂化类型是sp2、sp3,l mol三聚氰胺分子中含15molσ键.
(6)碳化硅的晶胞与金刚石的晶胞相似如图4,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为$\frac{2π({b}^{3}+{c}^{3})}{3{a}^{3}}$×100%.(用含a、b、c的式子表示).
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(2)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入AgNO3溶液时,无明显现象,往其溶液中加BaCl2溶液时若,产生白色沉淀,则该配合物的化学式为[Co(Br)(NH3)5]SO4,中心离子的配位数为6.
(3)参考下表中的物质熔点回答下列问题
| 物质 | NaF | NaCl | NaBr | NaI | NaCl | KCl | RbCl | CsCl |
| 熔点(℃) | 995 | 801 | 755 | 651 | 801 | 776 | 715 | 646 |
(4)C60可用作储氢材料.C60的结构如图1.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确不正确,并阐述理由C60是分子晶体,熔化时不需破坏化学键.科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体,该物质的K原子和C60分子的个数比为3:1.
 σ
σ(5)三聚氰胺分子的结构简式如图3,则其中氮原子轨道杂化类型是sp2、sp3,l mol三聚氰胺分子中含15molσ键.
(6)碳化硅的晶胞与金刚石的晶胞相似如图4,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为$\frac{2π({b}^{3}+{c}^{3})}{3{a}^{3}}$×100%.(用含a、b、c的式子表示).
17.下列各组元素中,属于同一周期的是( )
| A. | C、O、S | B. | Li、Na、K | C. | Si、P、Cl | D. | F、Cl、Br |
14.已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>b | B. | 氢化物的稳定性:H2Y<HZ | ||
| C. | 离子的还原性:Y2-<Z- | D. | 原子半径:r(X)<r(W) |
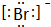 .
.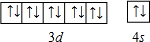 .
.