题目内容
16.纯碱是重要的化工厂产品,可用来制玻璃,制皂,造纸,纺织,印染等.其合成及其他综合利用过程如下图所示:
(1)图中制取的原料气体是N2、H2.原料气中的一种气体源于碳氢化合物和水.请写出甲烷和水在催化剂和高温条件下反应的方程式:CH4+2H2O$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO2+4H2或CH4+H2O$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO+3H2.
(2)工业生产中,设备A中发生的化学反应方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,母液中可提取的副产品是化学方程式是NH4Cl.
(3)尿素[CO(NH2)2]适用于各种土壤,在土壤中尿素发生水解,生成两种气体,其水解的化学方程式是CO(NH2)2+H2O=2NH3↑+CO2↑.
(4)纯碱的水溶液可用来洗涤油污,理由是CO32-+H2O
 HCO3-+OH-,溶液显碱性,促进油脂的水解(结合相关离子方程式解释).
HCO3-+OH-,溶液显碱性,促进油脂的水解(结合相关离子方程式解释).(5)上述流程中,可循环使用的物质是N2、H2、CO2、NaHCO3.
(6)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品NaCl的质量分数.样品W克$→_{溶液}^{H_{2}O}$溶液$→_{过滤}^{过量NaCl}$沉淀$→_{洗涤}^{H_{2}O}$$\stackrel{低温烘干,冷却,称量}{→}$固体m克样品中NaCl质量分数的表达式为(1-$\frac{106m}{197w}$)×100%.
分析 (1)合成氨的原料气是N2、H2;反应物为甲烷和水,条件是高温、催化剂,产物之一是氢气,甲烷完全燃烧产物是二氧化碳,不完全燃烧产物为一氧化碳,据此写出即可;
(2)依据反应原理推断设备A中的化学反应方程式,并得出副产物;
(3)依据尿素的化学式和题目所给的额信息结合化学反应原理写出化学反应方程式;
(4)纯碱是Na2CO3,是强碱弱酸盐,在溶液中水解显碱性,而油脂能在碱性条件下水解;
(5)根据流程图来分析;
(6)依据质量分数的计算方法,计算即可.
解答 解:(1)合成氨的原料气是N2、H2;依据题给的信息,甲烷与水在高温催化剂作用下生成二氧化碳(或一氧化碳)和氢气,故化学反应方程式为CH4+2H2O $\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO2+4H2或CH4+H2O$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO+3H2,故答案为:CH4+2H2O $\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO2+4H2或CH4+H2O$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$CO+3H2;
(2)在生产中,设备A中应生成目标产物纯碱,故发生的反应为:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓,由于NaHCO3是想得到的产品,故NH4Cl是副产品,故答案为:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓;NH4Cl;
(3)尿素的水解生成两种气体,结合尿素的元素组成,故生成的是氨气和二氧化碳,故反应为:CO(NH2)2+H2O=2NH3↑+CO2↑,故答案为:NaCl;CO(NH2)2+H2O=2NH3↑+CO2↑;
(4)纯碱是Na2CO3,是强碱弱酸盐,在溶液中水解显碱性:CO32-+H2O HCO3-+OH-,而油脂能在碱性条件下水解,故答案为:CO32-+H2O
HCO3-+OH-,而油脂能在碱性条件下水解,故答案为:CO32-+H2O HCO3-+OH-,溶液显碱性,促进油脂的水解;
HCO3-+OH-,溶液显碱性,促进油脂的水解;
(5)根据流程图可知,由于合成氨的反应是可逆反应,不能进行彻底,故N2、H2可以循环利用,NaHCO3及分解产生的CO2也可以循环利用,故答案为:N2、H2、CO2、NaHCO3;
(6)生成mg固体为BaCO3,其物质的量为:$\frac{mg}{197g/mol}$,则碳酸钠的质量为:$\frac{mg}{197g/mol}$×106g/mol=$\frac{106m}{197}$g,
故氯化钠的质量为(w-$\frac{106m}{197}$)g,则氯化钠的质量分数为:$\frac{w-\frac{106m}{197}}{w}$×100%=(1-$\frac{106m}{197w}$)×100%,
故答案为:(1-$\frac{106m}{197w}$)×100%.
点评 本题考查了纯碱的工业制法,题目难度较大,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及灵活应用基础知识的能力,明确合成原理为解答关键.

 综合自测系列答案
综合自测系列答案| A. | 金属元素与非金属元素能形成共价化合物 | |
| B. | 只有在原子中,质子数与核外电子数相等 | |
| C. | 目前使用的元素周期表中,最长的周期含有36种元素 | |
| D. | 氧和臭氧互为同位素 |
| A. | 把电能转变为化学能的装置 | |
| B. | 活泼金属做正极,不活泼金属或非金属做负极 | |
| C. | 外电路中电子从负极流向正极 | |
| D. | 正极发生氧化反应 |
| A. | ⅦA族元素形成的单质的熔点随元素原子序数增大而升高 | |
| B. | ⅦA族元素易形成-1价离子 | |
| C. | 最高价氧化物的水化物显酸性 | |
| D. | 从上到下气态氢化物的稳定性依次增强 |
| A. | CH3(CH2)2CH3 | B. | CH3(CH2)15CH3 | C. | CHCl3 | D. | CH4 |



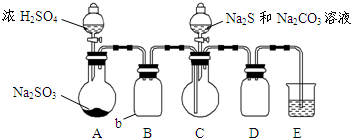 硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).