��Ŀ����
����Ŀ�������Ȼ�ѧ����ʽ�����ӷ���ʽ�У���ȷ���ǣ�
A.����ı�ȼ����Ϊ-890.3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ�� CH4��g��+2O2��g��=CO2��g��+2H2O��g�� ��H=-890.3kJ��mol-1
B.500�桢30MPa�£���0.5mol N2��1.5molH2�� ���ܱյĴ����г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��![]() ��H=-38.6kJ��mol-1
��H=-38.6kJ��mol-1
C.�Ȼ�þ��Һ�백ˮ��Ӧ��![]()
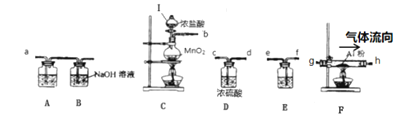
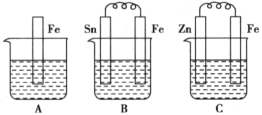
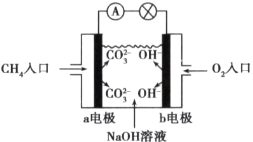
D.������ʴʱ���ܷ�����������Ӧ��2H2O+ O2+ 4e����4OHһ
���𰸡�D
��������
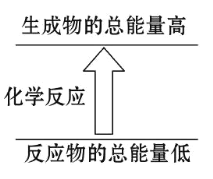
A��ȼ�����������ȶ��������ˮΪҺ̬ˮ����������̬ˮ����A����
B��0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3(g)������19.3kJ�����ɵİ��������ʵ���С��1mol�����Է�Ӧ![]() ����H��-38.6kJ��mol-1����B����
����H��-38.6kJ��mol-1����B����
C���Ȼ�þ��Һ�백ˮ��Ӧ�����ӷ���ʽΪMg2++2NH3��H2O=Mg(OH)2��+2NH4+����C����
D��������ʴʱ���ܷ���������ʴ����缫��ӦΪ��2H2O+O2+4e-=4OH-����D��ȷ��
�ʴ�ΪD��

��ϰ��ϵ�д�
 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����Ŀ