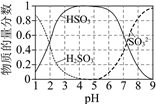题目内容
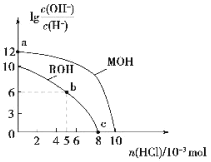
【题目】处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3、ClO、CNO(C+4价,N-3价)、Cl等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO+2CNO+H2O == N2+2HCO3+3Cl
D.每处理1 mol CNO转移3 mol e
【答案】A
【解析】
由图可知,ClO-浓度减小,HCO3-浓度增加,则还原反应为ClO-→Cl-,氧化反应为CNO-→N2,由电子、电荷守恒可知离子反应为3ClO-+2CNO-+H2O=N2↑+2HCO3-+3Cl-,以此来解答。
A.根据分析,离子反应为3ClO-+2CNO-+H2O=N2↑+2HCO3-+3Cl-,产物中含有碳酸氢根离子,碳酸氢根离子水解程度大于电离程度,使溶液显碱性。若溶液为强酸性,不可能含有HCO3-离子,故A错误;
B.对废水处理的目的本身就是将废水中的有害物质转化为对生态环境无害的物质,根据分析对废水处理发生的反应产物为N2、HCO3-、Cl-对环境无害,故B正确;
C.根据分析,废水处理发生的反应离子方程式为:3ClO+2CNO+H2O = N2+2HCO3+3Cl,故C正确;
D.根据分析,还原反应为ClO-→Cl-,Cl元素由+1价变为-1价,3mol ClO-可处理2mol CNO-,转移电子的物质的量=3mol×2=6mol,则每处理1 mol CNO转移3 mol e,故D正确;
答案选A。

练习册系列答案
相关题目