题目内容
【题目】下列实验操作和现象对应的结论错误的是
选项 | 实验操作和现象 | 结论 |
A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO32- |
B |
| 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO |
C | 向1mL浓度均为0.05mol·L-lNaCl、NaI的混合溶液中滴加2滴0.01mol·L-lAgNO3溶液,振荡,沉淀呈黄色 | Ksp(AgCl)<Ksp(AgI) |
D | 室温下,用pH试纸测得0.1mol·L-l NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
A. A B. B C. C D. D
【答案】C
【解析】A. 向溶液X中滴加BaCl2溶液,有白色沉淀生成,溶液X中可能含有SO42-、CO32-、SiO32-、SO32-等等,A正确;B.该实验中过量的铜和混酸发生反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,混酸中NO3-和H+ 的物质的量之比恰好为1:4,故反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO ,B正确; C. 向1mL浓度均为0.05mol·L-lNaCl、NaI的混合溶液中滴加2滴0.01mol·L-lAgNO3溶液,振荡,沉淀呈黄色,由于只有少量的AgNO3溶液,说明只有碘化银沉淀生成,故Ksp(AgCl)>Ksp(AgI),C不正确; D. HSO3-是弱酸的酸式根离子,其既能电离又能水解,室温下,用pH试纸测得0.1mol·L-l NaHSO3溶液的pH约为5,说明HSO3-的电离程度大于其水解程度,D正确。本题选C。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用铬,通常采用如下流程处理:
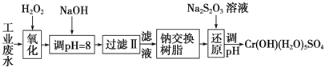
注:部分阳离子常温下沉淀时的pH见下表
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀pH | 1.4 | 7 | 9.1 | 3.4 | 4.3 |
完全沉淀pH | 3.7 | 9.6 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1)氧化过程主要是氧化Fe2+和Cr3+,氧化Fe2+的目的是:________________;其中Cr3+被氧化为Cr2O72-,该反应的离子方程式为:____________,氧化Cr3+的目的是__________。
(2)选择以下合适选项填空:加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR→MRn+nNa+,此步操作被交换除去的杂质离子是_____。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程中,氧化剂和还原剂的物质的量之比为:_________________。