题目内容
18.写出下列基团(或官能团)的名称或结构简式:名称:-CH2CH3乙基、-OH羟基、RCOOR′酯基、-X卤素原子
结构简式:醛基-CHO、羧基-COOH、双键-C=C-、三键-C≡C-.
分析 熟悉常见原子团的书写方法以及常见官能团的结构简式和名称即可轻松解答.
解答 解:-CH2CH3为乙基,-OH 为羟基,RCOOR′为酯基,-X为卤素原子;
醛基为-CHO,羧基为-COOH,双键-C=C-,三键-C≡C-,故答案为:乙基;羟基;酯基;卤素原子;-CHO;-COOH;-C=C-;-C≡C-.
点评 本题考查常见有机物的基团、官能团的结构名称的考查,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.有下列两组命题
B组中命题正确,且能用A组命题加以正确解释的是( )
| A组 | B组 |
| Ⅰ.H-F键键能小于H-Cl键键能 | ①HCl比HF稳定 |
| Ⅱ.H-I键键能小于H-Cl键键能 | ②HCl比HI稳定 |
| Ⅲ.HCl分子间作用力大于HF分子间作用力 | ③HCl沸点比HF高 |
| Ⅳ.HI分子间作用力小于HCl分子间作用力 | ④HI沸点比HCl低 |
| A. | Ⅰ① | B. | Ⅱ② | C. | Ⅲ③ | D. | Ⅳ④ |
3.经测定,由C3H7OH、C2H5OC2H5和C6H12组成的混合物中氧的质量分数为8%,则此混合物中氢的质量分数为( )
| A. | 78% | B. | 22% | C. | 14% | D. | 13% |
6.软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4•H2O的流程如下:

已知:①部分金属阳离子完全沉淀时的pH如下表
②温度高于27℃时,MnSO4晶体的溶解度随温度的升高而逐渐降低.
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为SO2+MnO2═Mn2++SO42-;
(2)第1步除杂中加入H2O2的目的是将Fe2+氧化为Fe3+.
(3)第1步除杂中形成滤渣l的主要成分为Al(OH)3、Fe(OH)3(填化学式),调pH至5-6所加的试剂,可选择a、b(填以下试剂的序号字母); a.Cao b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式MnF2+Mg2+═Mn2++MgF2,该反应的平衡常数数值为7.2×107.
(已知:MnF2的Ksp=5.3×10-3;CaF2的Ksp=1.5×10-10;MgF2的Ksp=7.4×10-11):
(5)采用“趁热过滤”操作的原因是因为减少MnSO4•H2O在水中的溶解,得到更所得产品.
(6)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是Mn2++2H2O?Mn(OH)2+2H+(用离子方程式表示),该溶液中所有离子的浓度由大到小的顺序为c(SO42-)>c(Mn2+)>c(H+)>c(OH-).

已知:①部分金属阳离子完全沉淀时的pH如下表
| 金属阳离子 | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的PH值 | 3.2 | 5.2 | 10.4 | 12.4 |
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为SO2+MnO2═Mn2++SO42-;
(2)第1步除杂中加入H2O2的目的是将Fe2+氧化为Fe3+.
(3)第1步除杂中形成滤渣l的主要成分为Al(OH)3、Fe(OH)3(填化学式),调pH至5-6所加的试剂,可选择a、b(填以下试剂的序号字母); a.Cao b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式MnF2+Mg2+═Mn2++MgF2,该反应的平衡常数数值为7.2×107.
(已知:MnF2的Ksp=5.3×10-3;CaF2的Ksp=1.5×10-10;MgF2的Ksp=7.4×10-11):
(5)采用“趁热过滤”操作的原因是因为减少MnSO4•H2O在水中的溶解,得到更所得产品.
(6)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是Mn2++2H2O?Mn(OH)2+2H+(用离子方程式表示),该溶液中所有离子的浓度由大到小的顺序为c(SO42-)>c(Mn2+)>c(H+)>c(OH-).
13.下列物质属于芳香烃,但不是苯的同系物的是( )
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
| A. | ③④ | B. | ②⑤⑥ | C. | ①②⑤⑥ | D. | ②③④⑤⑥ |
3.下列实验装置或操作设计正确且能达到实验目的是( )
| A. | 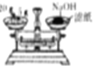 称量NaOH固体 | B. | 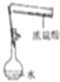 配制一定物质的量浓度稀硫酸 | ||
| C. | 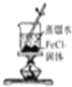 制取少量的Fe(OH)3胶体 | D. | 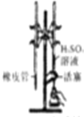 用H2SO4标准溶液滴定NaOH溶液 |
10.下列说法正确的是( )
| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| B. | 棉、丝、羽毛、塑料及合成橡胶完全燃烧都只生成CO2和H2O | |
| C. | 纤维素、合成纤维、光导纤维都是有机高分子化合物 | |
| D. | 液化石油气可由石油分馏获得,汽油可由石油分馏或石油裂化获得 |
7.由下列实验现象得出的结论正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 取某Na2SO3溶液,加入足量的稀盐酸,产生气泡,再滴加BaCl2溶液,产生白色沉淀. | Na2SO3已部分被氧化 |
| B | 向2mL0.1mol/LNaOH溶液中滴加0.1mol/LMgCl2溶液3滴,出现白色沉淀后,再滴加3滴0.1mol/L FeCl3溶液,出现红褐色沉淀. | 溶解度:Mg(OH)2>Fe(OH)3 |
| C | 向氯水中通入足量SO2,氯水褪色. | SO2具有漂白性 |
| D | 相同温度下,测等浓度的Na2CO3和Na2SO3水溶液的pH:pH (Na2CO3)>pH(Na2SO3). | 非金属性强弱:C>S |
| A. | A | B. | B | C. | C | D. | D |
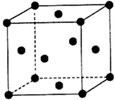 W、X、Y、Z(W、X、Y、Z分别代表元素符号)均为元素周期表中前四周期的元素,其原子序数依次增大,其中W、X、Y为短周期元素,它们的单质在通常状况下均为无色气体.X元素的基态原子在同周期元素基态原子中含有的未成对电子数最多,Y元素的基态原子中s能级上的电子数等于p能级上的电子数,Z为金属元素,其基态原子是具有4s1结构的基态原子中质子数最多的原子,试回答下列各题:
W、X、Y、Z(W、X、Y、Z分别代表元素符号)均为元素周期表中前四周期的元素,其原子序数依次增大,其中W、X、Y为短周期元素,它们的单质在通常状况下均为无色气体.X元素的基态原子在同周期元素基态原子中含有的未成对电子数最多,Y元素的基态原子中s能级上的电子数等于p能级上的电子数,Z为金属元素,其基态原子是具有4s1结构的基态原子中质子数最多的原子,试回答下列各题: