题目内容
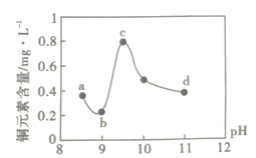
【题目】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。查阅资料:
平衡Ⅰ:Cu(OH)2+4NH3![]() [Cu(NH3)4]2+2OH-
[Cu(NH3)4]2+2OH-
平衡Ⅱ:Cu(OH)2+2OH-![]() [Cu(OH-)4]2-
[Cu(OH-)4]2-
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/mg·L-1 | 72 | ≤0.5 |
Nh4+/mg·L-1 | 2632 | ≤15 |
下列说法错误的是( )
A.a~b段发生的反应为:Cu2++2OH-=Cu(OH)2↓
B.b~c段:随pH升高,Cu(OH)2的量增加,导致平衡Ⅰ正向移动,铜元素含量上升
C.c~d段:随pH升高,c(OH-)增加,平衡Ⅰ逆向移动,铜元素含量下降
D.d点以后,随c(OH-)增加,铜元素含量可能上升
【答案】B
【解析】
滴加NaOH(aq)的过程中依次发生过些Ⅰ:2OH-+Cu2+=Cu(OH)2(a>b):过程Ⅱ:NH4++OH-=NH3+H2O2NH3使平衡Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-正向移动(b→c);过程Ⅲ:继续滴加,OH-便Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH游向移动(e→d)若NaOH继续过量滴加可使Cu(OH)2+2OH=[Cu(OH)4]2正向移动(d点之后)。
A、图象中的变化曲线可知PH=9时铜离子浓度最小,废水中Cu2+处理的最佳pH约为9,故A正确;
B、b~c段随氢氧根离子浓度增大,铵根离子与氢氧根离子结合生成一水合氨,氨气浓度增大,Cu(OH)2+4NH3=[Cu(NH3)4]2++20H-,平衡正向进行,溶液中通过离子浓度增大,故B错误;
C、c~d段,随氢氧根离子浓度的增大,Cu(OH)2+4NH3=[Cu(NH3)4]2++20H-逆向进行,铜离子浓度减小,铜元素含量下降,故C正确;
D、d点以后,随c(OH-)增加,平衡II:Cu(OH)2+2OH-=[Cu(OH)4]2-正向进行,上层清液中铜元素的含量可能上升,故D正确;
故答案为:B。