题目内容
2.根据表中信息,判断下列叙述中正确的是( )| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeI2 | I2 | ||
| ② | KClO3 | 浓盐酸 | Cl2 | ||
| ③ | KMnO4 | H2O2 | O2 | Mn2+ |
| A. | 表中①组的反应中氧化产物一定是I2 | |
| B. | 氧化性强弱的比较:KClO3>Cl2>Fe3+>I2 | |
| C. | 表中②组每生成1molCl2,转移1mol电子 | |
| D. | 表中③组其他反应物可以为浓盐酸 |
分析 ①过量的氯气与碘化亚铁反应为2FeI2+3Cl2═2FeCl3+2I2,Cl元素化合价降低,被还原,Fe、I元素化合价升高,被氧化,
②KClO3+6HCl═KCl+3Cl2↑+3H2O,KClO3中Cl元素化合价降低,被还原,HCl中Cl元素化合价升高,被氧化,
③5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,Mn元素化合价降低,被还原,O元素化合价升高,被氧化,结合氧化还原反应的有关概念解答该题.
解答 解:A.表中①组的反应中氧化产物是FeCl3和I2,故A错误;
B.氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,则氧化性强弱的比较:KClO3>Cl2>Fe3+>I2,故B正确;
C.KClO3+6HCl═KCl+3Cl2↑+3H2O,KClO3中Cl元素化合价从+5价降低到0价,转移5个电子,则每生成1molCl2,转移$\frac{5}{3}$mol电子,故C错误;
D.KMnO4能氧化浓盐酸,所以不能用浓盐酸酸化,故D错误.
故选B.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,明确元素化合价变化是解本题关键,知道常见元素化合价,知道元素性质与化合价的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列化学实验事实及其解释或结论都正确的是( )
| A. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| B. | 向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再加入0.5 mL有机物X,加热后未出现砖红色沉淀,说明X中不含有醛基 | |
| C. | 向CuSO4溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振荡,四氯化碳层呈紫色,说明白色沉淀可能为CuI | |
| D. | 向浓度均为0.1 mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,首先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
10.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA | |
| B. | 18g D2O含有的电子数为10NA | |
| C. | 在标准状况下,22.4LSO3的物质的量为1mol | |
| D. | 同温、同压下,相同体积的氟气和氩气所含的原子数相等 |
17.下列实验操作或装置(略去部分加持仪器)正确的是( )
| A. |  如图表示为配制一定物质的量浓度稀硫酸时的操作 | |
| B. |  如图表示为配制一定物质的量浓度的溶液定容时的操作 | |
| C. | 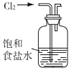 用如图所示装置吸收氯气中的氯化氢气体 | |
| D. | 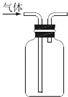 用图所示装置收集一氧化氮气体 |
14.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?若a=7,则HA是强酸;若a>7,则HA是弱酸.
(2)若考虑其他组的实验结果,则c1>(填“<”、“>”或“=”)0.2mol•L-1;乙组实验中HA和NaOH溶液混合前,HA溶液中C(A-)与NaOH溶液中C(Na+)的关系是B
A.前者大 B.后者大 C.二者相等 D.无法判断.
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);其中,C(A-)=0.1+1×10-9-1×10-5mol•L-1(不能做近似计算,回答准确值,结果不一定要化简).
(4)丁组实验中,HA和NaOH溶液混合前后C(HA)>(填“<”、“>”或“=”)C(NaOH);b<7(填“<”、“>”或“=”)
| 实验编号 | HA | NaOH | 混合后溶液的pH |
| 甲 | C(HA)=0.2mol•L-1 | C(NaOH)=0.2mol•L-1 | pH=a |
| 乙 | C(HA)=c1mol•L-1 | C(NaOH)=0.2mol•L-1 | pH=7 |
| 丙 | C(HA)=0.1mol•L-1 | C(NaOH)=0.1mol•L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?若a=7,则HA是强酸;若a>7,则HA是弱酸.
(2)若考虑其他组的实验结果,则c1>(填“<”、“>”或“=”)0.2mol•L-1;乙组实验中HA和NaOH溶液混合前,HA溶液中C(A-)与NaOH溶液中C(Na+)的关系是B
A.前者大 B.后者大 C.二者相等 D.无法判断.
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);其中,C(A-)=0.1+1×10-9-1×10-5mol•L-1(不能做近似计算,回答准确值,结果不一定要化简).
(4)丁组实验中,HA和NaOH溶液混合前后C(HA)>(填“<”、“>”或“=”)C(NaOH);b<7(填“<”、“>”或“=”)
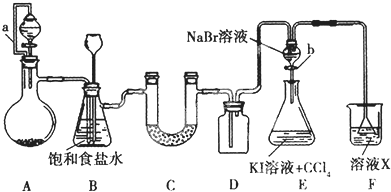
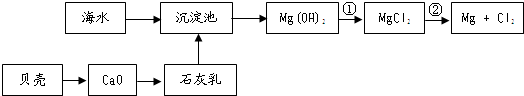
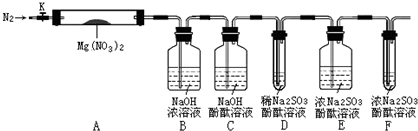
 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.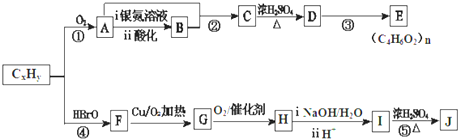

 .
.