题目内容
14.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:| 实验编号 | HA | NaOH | 混合后溶液的pH |
| 甲 | C(HA)=0.2mol•L-1 | C(NaOH)=0.2mol•L-1 | pH=a |
| 乙 | C(HA)=c1mol•L-1 | C(NaOH)=0.2mol•L-1 | pH=7 |
| 丙 | C(HA)=0.1mol•L-1 | C(NaOH)=0.1mol•L-1 | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?若a=7,则HA是强酸;若a>7,则HA是弱酸.
(2)若考虑其他组的实验结果,则c1>(填“<”、“>”或“=”)0.2mol•L-1;乙组实验中HA和NaOH溶液混合前,HA溶液中C(A-)与NaOH溶液中C(Na+)的关系是B
A.前者大 B.后者大 C.二者相等 D.无法判断.
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);其中,C(A-)=0.1+1×10-9-1×10-5mol•L-1(不能做近似计算,回答准确值,结果不一定要化简).
(4)丁组实验中,HA和NaOH溶液混合前后C(HA)>(填“<”、“>”或“=”)C(NaOH);b<7(填“<”、“>”或“=”)
分析 (1)酸碱恰好完全反应,如反应后呈中性,则pH=7,为强酸,如pH>7,则为弱酸;
(2)根据丙可知,HA为弱酸,当c1=0.2mol/L时,溶液呈碱性,若为中性,则c1大于0.2mol/L;HA为弱酸,电离程度较小,只能部分电离出A-;
(3)pH>7,所以HA是弱酸,结合电荷守恒判断各离子浓度大小;根据电荷守恒及溶液pH计算出c(A-);
(4)HA为弱酸,反应前酸的浓度大于氢氧化钠浓度,则混合液中酸过量,溶液呈酸性.
解答 解:(1)不考虑其它组的实验结果,单从甲组情况分析,若a=7,说明反应生成强酸强碱盐,则HA是强酸;若a>7,说明反应生成强碱弱酸盐,则HA是弱酸,
故答案为:若a=7,则HA是强酸;若a>7,则HA是弱酸;
(2)根据丙恰好反应生成NaA溶液呈碱性可知,HA为弱酸,若溶液为中性,则c1大于0.2mol/L;
由于HA为弱酸,电离程度较小,则HA溶液中c(A-)小于c(Na+),即B正确,
故答案为:>;B;
(3)HA物质的量浓度为0.1mol/L,NaOH物质的量浓度为0.1mol/L,二者恰好反应生成NaA,由于pH>7,则c(OH-)>c(H+),根据电荷守恒c(OH-)+c(A-)=c(Na+)+c(H+)可知:c(Na+)>c(A-),则溶液中离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+);
根据电荷守恒可知:c(OH-)+c(A-)=c(Na+)+c(H+),则c(A-)=c(Na+)+c(H+)-c(OH-)=0.1mol/L+1×10-9mol/L-1×10-5mol/L,
故答案为:c(Na+)>c(A-)>c(OH-)>c(H+);0.1+1×10-9-1×10-5;
(4)pH=2的HA溶液中,由于HA为弱酸,则HA的浓度大于0.01mol/L,pH=12的氢氧化钠溶液的浓度为0.01mol/L,则HA的浓度大于氢氧化钠溶液的浓度;混合液中酸过量,溶液呈酸性,则溶液的pH=b<7,
故答案为:>;<.
点评 本题考查较为综合,涉及了盐类水解、强弱电解质的判断、电荷守恒等知识,有一定的综合性,为高考常见题型,题目难度中等,侧重于学生的分析能力和计算能力的考查,该题的命题方式为高考命题的热点.

| A. | 稀硝酸、稀硫酸 | B. | 硝酸银溶液 | C. | 浓硝酸、浓硫酸 | D. | 硫酸铜溶液 |
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeI2 | I2 | ||
| ② | KClO3 | 浓盐酸 | Cl2 | ||
| ③ | KMnO4 | H2O2 | O2 | Mn2+ |
| A. | 表中①组的反应中氧化产物一定是I2 | |
| B. | 氧化性强弱的比较:KClO3>Cl2>Fe3+>I2 | |
| C. | 表中②组每生成1molCl2,转移1mol电子 | |
| D. | 表中③组其他反应物可以为浓盐酸 |
| A. | 若生成物C和D分别为盐和水,则该反应一定是中和反应 | |
| B. | 若A和C是单质,B和D是化合物,则该反应一定是置换反应 | |
| C. | 若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀 | |
| D. | 若A是可溶性碱,B是可溶性盐,则C和D一定是另一种碱和另一种盐 |

| A. | 盐酸与烧碱反应 | B. | 铁丝与氯气反应 | C. | 氧化钙和水反应 | D. | 碳酸钙分解反应 |

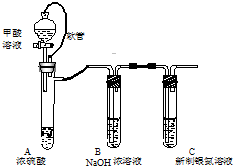 银氨溶液可用于检测CO气体,实验室研究的装置如图:
银氨溶液可用于检测CO气体,实验室研究的装置如图: