题目内容
【题目】如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、C1-)生产CuCl的流程:
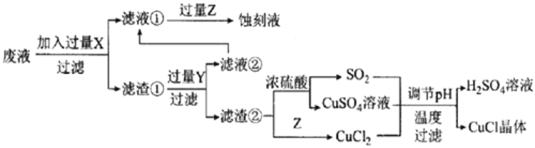
已知:CuCl是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化为绿色,见光分解变成褐色。
请回答下列问题:
(1)流程中的滤渣①与Y反应和X与Y反应相比,单位时间内得到的气体多,其原因为____________________________________________。
(2)滤液①需要加过量Z,检验Z过量的方法是______________________。
(3)写出生成CuCl的离子方程式:_________________________________。
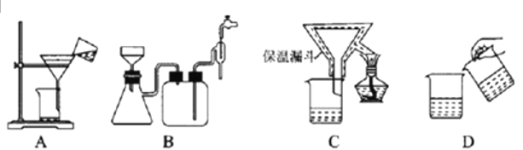
(4)为了提高CuCl产品的纯度,流程中的“过滤”操作适宜用下列装置图中的___________(填选项字母),过滤后,洗涤CuCl的试剂宜选用___________(填“无水乙醇”或“稀硫酸”)
(5)CuCl加入饱和NaCl溶液中会部分溶解生成CuCl2-,在一定温度下建立两个平衡:
I. CuCl (s) ![]() Cu +(aq)+Cl- (aq) Ksp=1.4×10-6
Cu +(aq)+Cl- (aq) Ksp=1.4×10-6
II. CuCl(s)+Cl- (aq)![]() CuCl2-(aq) K=0.35。
CuCl2-(aq) K=0.35。
分析c(Cu+)、c(CuCl2-)和Ksp、K的数学关系,在图中画出c(Cu+)、c(CuCl2-)的关系曲线(要求至少标出一个坐标点) ______。

(6)氯化亚铜的定量
①称取样品0.25g于250mL锥形瓶中,加入10mL过量的FeCl3溶液,不断摇动:
②待样品溶解后,加入20mL蒸馏水和2滴指示剂;
③立即用0.1000mol·L-1硫酸铈标准溶液滴定至绿色为终点;
④重复三次,消耗硫酸铈溶液的平均体积为24.30mL。
上述相应化学反应为CuCl+ FeCl3===CuCl2+FeCl2、Fe2++Ce4+===Fe3++Ce3+,则样品中CuCl的纯度为___________(保留三位有效数字)。
【答案】滤渣①中有铁和铜,与盐酸反应时形成无数微小的原电池,极大地加快了反应速率 取溶液少量,加入KBr溶液少量和四氯化碳,如下层液体呈橙色,说明氯气已过量(其他合理答案均可) CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4 B 无水乙醇 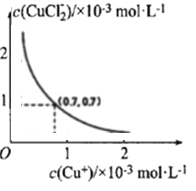 96.7%
96.7%
【解析】
废液中加入过量铁粉,发生反应:Fe+2Fe3+=3Fe2+、 Fe+Cu2+=Fe2++Cu,原溶液中的Fe3+、Cu2+被除去,过滤所得的滤液①中含有Fe2+、Cl-,在滤液中加入过量的氯气,可以将Fe2+氧化成FeCl3,即得到FeCl3蚀刻液,实现蚀刻液的再生。滤渣为铜单质和剩余的铁单质,加入过量的稀盐酸,铜与稀盐酸不反应,因此滤液②也为FeCl2溶液,滤渣②为铜。
(1)流程中的滤渣①与Y反应和X与Y反应相比,单位时间内得到的气体多,说明反应速率快,因为滤渣①中有铁和铜单质,与盐酸反应时能形成无数微小的原电池,极大地加快了反应速率;(2)检验溶液中通入的氯气已过量,可取溶液少量,加入KBr溶液少量和四氯化碳,如下层液体呈橙色,说明氯气已过量。(3)根据流程图可知,SO2、CuSO4、CuCl2反应生成H2SO4、CuCl,因此化学方程式为:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4。
(4)生产中为了提高CuCl产品的质量,尽可能减少CuCl被空气中氧气氧化,宜采用抽滤法快速过滤,所以过滤装置选择B项。洗涤CuCl宜选用无水乙醇,因为CuCl难溶于无水乙醇,洗涤时可减少CuCl的溶解损失,而且后续干燥中易除去乙醇。不选用硫酸,虽然CuCl难溶于硫酸,但用硫酸洗涤,会给CuCl表面带来少量的H+和SO42-杂质。
(5)据反应式CuCl(s)+Cl- (aq)![]() CuCl2-(aq)和K的本义式有:
CuCl2-(aq)和K的本义式有:
![]() ,将分子、分母同乘以c(Cu+)得:
,将分子、分母同乘以c(Cu+)得:
![]() ,将题给的K和Ksp的数据代入得c(CuCl2-)×c(Cu+)=1.4×10-6×0.35=4.9×10-7。取其中(0.7,0.7)做为一个坐标点,图象示意如下:
,将题给的K和Ksp的数据代入得c(CuCl2-)×c(Cu+)=1.4×10-6×0.35=4.9×10-7。取其中(0.7,0.7)做为一个坐标点,图象示意如下:

(6)根据题给的相应化学反应CuCl+ FeCl3===CuCl2+FeCl2、Fe2++Ce4+===Fe3++Ce3+,可得
CuCl和Ce4+的反应配比是1:1,所以可得CuCl的纯度:![]() =96.7%。
=96.7%。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
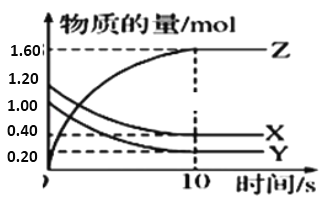
名题训练系列答案【题目】在2 L密闭容器中,800℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)已知:K(300℃)>K(350℃),该反应是____热反应。
(2)如图中表示NO2浓度变化曲线的是__(填序号),用O2表示从0~2 s内该反应的平均速率v=___。
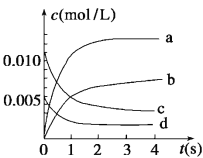
(3)能说明该反应已经达到平衡状态的是__(填字母序号)。
a.c(NO2)=2c(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是___(填字母序号)。
a.及时分离出NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效的催化剂