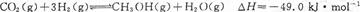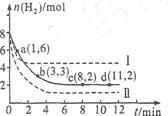题目内容
下列说法正确的是
| A.常温下能够进行的化学反应都是放热反应,高温下进行的反应都是吸热反应 |
| B.常温常压下,pH = 1的盐酸中约含有6.02×1023个氢离子 |
| C.常温常压下,0.5mol氮气和氢气的混合气体体积大于11.2L |
| D.原电池装置的正、负极可以是同一种金属 |
CD
A不正确,反应是放热反应还是吸热反应,与反应条件无关系,只与反应物和生成物总能量的相对大小有关系;B中溶液的体积无法确定,因此不能计算氢离子的物质的量,B不正确;根据PV=nTR可知,在压强不变时,气体体积随温度的升高而增大,C正确;D正确,例如燃料电池等,答案选CD。

练习册系列答案
相关题目
 CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H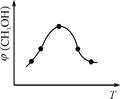
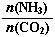 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为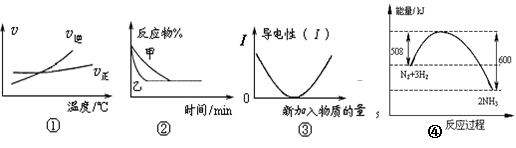
 2AB3(g)” 的ΔH>0
2AB3(g)” 的ΔH>0 7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是 L。
7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是 L。 CH3OH(g),达平衡后测得各组分浓度如下:
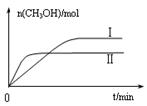
CH3OH(g),达平衡后测得各组分浓度如下: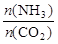 =4时,CO2的转化率随时间的变化关系如右图所示。
=4时,CO2的转化率随时间的变化关系如右图所示。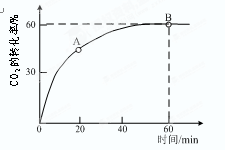
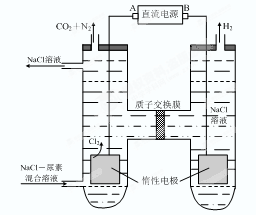
 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0