题目内容
13.下列离子方程式正确的是( )| A. | 实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯乙酸与氢氧化钠溶液共热:CH2ClCOOH+OH-→CH2ClCOO-+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O |
分析 A.醋酸在离子反应中保留化学式;
B.-Cl、-COOH均与NaOH反应;
C.反应生成苯酚和碳酸氢钠;
D.发生银镜反应,生成乙酸铵、水、银、氨气.
解答 解:A.实验室用大理石与醋酸反应制取二氧化碳的离子反应为:CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O,故A错误;
B.氯乙酸与氢氧化钠溶液共热的离子反应为CH2ClCOOH+2OH-→CH2OHCOO-+Cl-+H2O,故B错误;
C.苯酚钠溶液中通入少量二氧化碳的离子反应为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D.用银氨溶液检验乙醛中的醛基的离子反应为CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,选项C为解答的易错点,注意有机物官能团与性质的关系,题目难度不大.

练习册系列答案
相关题目
3.四种短周期元素在元素周期表中的位置如图,其中Z的原子半径最小.下列说法正确的是( )
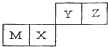

| A. | M元素一定为金属元素 | |
| B. | X元素的最简单气态氢化物的热稳定性比Z的强 | |
| C. | 若Y元素存在最高价含氧酸,其酸性比X元素的最高价含氧酸弱 | |
| D. | Z元素与氢元素能形成原子个数比为1:1的共价化合物 |
4.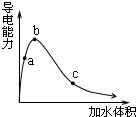 一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )
 一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )| A. | a、b、c三点醋酸的电离程度:c<a<b | |
| B. | a、b、c三点醋酸电离平衡常数:c<a<b | |
| C. | a、b、c三点溶液中的CH+:c<a<b | |
| D. | a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b |
8.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料.下列实验事实与硝酸性质不相对应的一组是( )
| A. | 浓硝酸使紫色石蕊试液先变红后褪色--酸性和强氧化性 | |
| B. | 不能用稀硝酸与锌反应制氢气--强氧化性 | |
| C. | 要用棕色瓶盛装浓硝酸--不稳定性 | |
| D. | 稀硝酸能使滴有酚酞的氢氧化钠溶液红色褪去--强氧化性 |
18.下列叙述中,不正确的是( )
| A. | 共价化合物中不可能含有离子键 | |
| B. | 硫酸分子中有H+和SO42-两种离子 | |
| C. | 某元素原子的最外层只有一个电子,它跟卤素可能形成离子键,也可能形成共价键 | |
| D. | 离子键和共价键的实质都是电性的相互作用 |
5.在2L密闭容器中,在一定条件下发生A+3B?2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则ν(A)为( )
| A. | 0.04mol/(L•s) | B. | 0.08mol/(L•s) | C. | 0.4mol/(L•s) | D. | 0.8mol/(L•s) |
2.下列表示物质的图或式正确的是( )
| A. | 氮气的电子式N┇┇N | B. | Mg2+的结构示意图 | ||
| C. | NH3的结构式 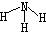 | D. | 甲基的电子式 |
3.下列各组离子在指定溶液中肯定大能量共存的是( )
| A. | 石蕊溶液呈蓝色的溶液:K+、Na+、NO3-、Cl- | |
| B. | 无色透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3- | |
| D. | 酸性溶液中:Al3+、Na+、SO42-、HCO3- |
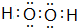 .固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-.
.固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-.