题目内容
【题目】常温下,向100mL0.01mol·L-1HA溶液中逐滴加入0.02mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
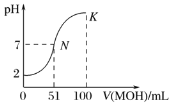
(1)由图中信息可知HA为________(填“强”或“弱”)酸,MOH为_________(填“强”或“弱”)碱。
(2)常温下一定浓度的MA稀溶液的pH=a,则a______(填“>”“<”或“=”)7,用离子方程式表示其原因:__________________,此时溶液中由水电离出的c(OH-)=____________。
(3)K点对应的溶液中,c(M+)+c(MOH)________(填“>”“<”或“=”)2c(A-),溶液中离子浓度的大小关系:__________________________。
【答案】强 弱 < M++H2O![]() MOH+H+ 1×10-amol·L-1 = c(M+)>c(A-)>c(OH-)>c(H+)
MOH+H+ 1×10-amol·L-1 = c(M+)>c(A-)>c(OH-)>c(H+)
【解析】
(1)根据图像可知,初始时,0.01mol/LHA溶液的pH=2,HA完全电离产生0.01mol/L的氢离子;生成的MA为强酸弱碱盐;
(2)MA为强酸弱碱盐,在溶液中发生M++H2O![]() MOH+H+;
MOH+H+;
(3)K点为MA、MOH的混合液,且物质的量相等,根据物料守恒判断。
(1)根据图像可知,未加入MOH时,0.01mol/LHA溶液的pH=2,HA完全电离产生0.01mol/L的氢离子,则HA为强酸;用0.02mol·L-1MOH溶液50mL时,恰好完全反应,溶液的pH<7,则生成的MA为强酸弱碱盐,MOH为弱碱;
(2)MA为强酸弱碱盐,在溶液中M++H2O![]() MOH+H+,则其稀溶液的pH=a,a<7;此溶液中,水电离出的氢离子与氢氧根离子的量相等,则c(OH-)=c(H+)=10-amol/L;
MOH+H+,则其稀溶液的pH=a,a<7;此溶液中,水电离出的氢离子与氢氧根离子的量相等,则c(OH-)=c(H+)=10-amol/L;
(3)K点加入MOH的体积为100mL,则MOH的物质的量为HA的2倍,混合后溶液为MA、MOH的混合液,且物质的量相等,根据物料守恒,则c(M+)+c(MOH)=2c(A-);溶液显碱性,则离子浓度由大到小的顺序为c(M+)>c(A-)>c(OH-)>c(H+)。