��Ŀ����
����Ŀ�����й�������ˮ���˵���������(����)
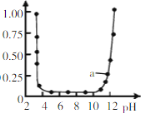
A.pH��ȵĢ�NaHCO3����Na2CO3����NaOH��Һ�����ʵ���Ũ�ȴ�С���٣��ڣ���
B.Ũ�Ⱦ�Ϊ0.1 mol��L��1�Ģ�(NH4)2CO3����(NH4)2SO4����(NH4)2Fe(SO4)2��Һ�У�c(NH4+)�Ĵ�С˳��Ϊ�٣��ڣ���
C.��NH4Cl��Һ�м���ϡHNO3��������NH4+ˮ��
D.��CH3COONa��Һ�м�������ᣬ������CH3COO��ˮ��
���𰸡�B
��������
A��pH��ȵĢ�NaHCO3����Na2CO3����NaOH����Һ����Խǿ��Ҫ��ҺŨ��ԽС����Һ�����ʵ���Ũ�ȴ�С���٣��ڣ��ۣ���A��ȷ��
B��(NH4)2CO3 ��CO32-�ٽ�NH4+ˮ�⣬(NH4)2Fe(SO4)2��Fe2+����NH4+ˮ�⣬�����ͬŨ�ȵ��⼸����Һ��笠�����Ũ�ȴ�С˳���Ǣۣ��ڣ��٣���B����
C����NH4Cl��Һ��笠�����ˮ����Һ�����ԣ�NH4++H2O=NH3H2O+H+������ϡHNO3��������Ũ������ƽ�������ƶ�������NH4+ˮ�⣬��C��ȷ��
D����������Һ�У����������ˮ�⣬CH3COO-+H2O![]() CH3COOH+OH-����Һ�Լ��ԣ���������ᣬ����Ũ������ˮ��ƽ�������ƶ�������CH3COO-ˮ�⣬��D��ȷ��
CH3COOH+OH-����Һ�Լ��ԣ���������ᣬ����Ũ������ˮ��ƽ�������ƶ�������CH3COO-ˮ�⣬��D��ȷ��
��ѡB��

����Ŀ���ж������ڴ�������Т�~����Ŷ�Ӧλ�û����̡�������������
��1��2020��6��23��9ʱ43�ֱ���ϵͳ����ʮ��ŵ��������߱����������һ��ȫ���������dzɹ����䣡ִ�б��η�������ij��������ػ����װ�ij���ȼ��Ϊƫ�����£�C2H8N2����������������ƫ�����º�����������Ҳ������Ϊȼ�ϵ�ص�������Ӧ����߷�Ӧ�IJ�����Ի�����������Ⱦ������������Ϣ�ж�����˵������
��ƫ���������л�����е�Ԫ�ػ��ϼ�Ϊ-3_____
������1molCO2ת��8mol����_____
��ƫ�������������������ķ�Ӧ�Ƿ��ȷ�Ӧ_____
�ܸ�ȼ�ϵ����ƫ�������Ǹ�����Ӧ��_____
��2����ͼ��ʾװ�ã������ɵ��������Ҷ�ȩ�Ʊ��Ҷ��ᣬ��Ӧԭ��Ϊ![]() ��2Cl2��2H2O��
��2Cl2��2H2O��![]() ��4HCl��
��4HCl��
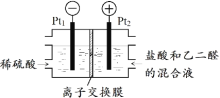
�ж�����˵��������
�ݸ�װ������������Ӧ������ȫ��ת��Ϊ��ѧ��_____
��Pt1�缫�ķ�ӦʽΪ2H2O��2e-=H2����2OH-_____
���������ǿ��Һ�����Ե����ã����ṩCl-����缫��Ӧ_____
��������ÿ�õ�0.1mol�Ҷ��ᣬ����0.4molH+������Ǩ�Ƶ�����_____
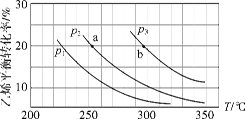
��3���ж϶�����ͼ�������������
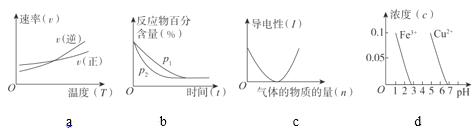
�����ͼa���жϷ�ӦA2(g)��3B2(g)![]() 2AB3(g)����H��0_____
2AB3(g)����H��0_____
��ͼb�ɱ�ʾѹǿ��P���Է�Ӧ2A(g)��2B(g)![]() 3C(g)��D(s)��Ӱ��_____
3C(g)��D(s)��Ӱ��_____
ͼc�ɱ�ʾ�������Һͨ�백��ʱ����Һ�������氱�����ı仯_____
����ͼd����ȥCuSO4��Һ�е�Fe3+���ɼ���NaOH����pH��3~4_____
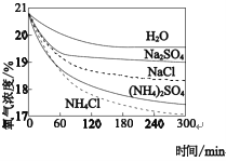
��4����������ʵ��̽�������ڲ�ͬ��Һ�е�������ʴ��
ʵ��װ�� | ʵ���� | ����Һ | pH | ����Ũ����ʱ��ı仯 |
| i | H2O | 7 |
|
ii | 1.0mol��L-1NH4Cl | 5 | ||
iii | 0.5mol��L11(NHspan>4)2SO4 | 5 | ||
iv | 1.0mol��L-1NaCl | 7 | ||
v | 0.5mol��L-1Na2SO4 | 7 |
ͨ������ʵ���ж�����˵������
i��iv��v�Ƚ�˵������Һ���Լӿ�������ʴ����_____
ii��iii��iv��v�Ƚ�˵��������ʴ������������������_____
��ʵ��v��Һ�м�������(NH4)2SO4���壬������ʴ���ʼӿ�_____
��ʵ��ii��Һ�мӵ������0.5mol��L-1(NH4)2SO4��������ʴ����һ���ӿ�_____
����Ŀ��ijͬѧ��ʵ���ҽ����������������ת��ʵ�顣
ʵ���Fe3+ת��ΪFe2+

(1)Fe3+��Cu�۷�����Ӧ�����ӷ���ʽΪ_________________________________��
(2)ijѧ���öԱ�ʵ�鷨̽����ɫ����������ԭ������дʵ����
ʵ�鷽�� | ���� | ���� |
����1��ȡ4mL��__________ mol/LCuSO4��Һ,�����еμ�3��0.1mol/LKSCN��Һ | ������ɫ���� | CuSO4��Һ��KSCN��Һ��Ӧ�����˰�ɫ���� |
����2��ȡ4mL��__________mol/LFeSO4 ��Һ�����еμ�3��0.1mol/LKSCN��Һ | ���������� |
�������ϣ�
��֪����SCN-�Ļ�ѧ������I-���� ��2Cu2++4I-=2CuI��+I2
Cu2+��SCN-��Ӧ�����ӷ���ʽΪ��___________________________________��
ʵ���Fe2+ת��ΪFe3+
ʵ�鷽�� | ���� |
��3mL0.1mol/LFeSO4��Һ�м���3mL0.5mol/Lϡ���� | ��Һ��Ϊ��ɫ������һ��ʱ�����ɫ��ʧ����Һ��Ϊ��ɫ |
̽������������ֵ�ԭ��
�������ϣ�Fe2++NO![]() Fe(NO)2+(��ɫ)
Fe(NO)2+(��ɫ)
(3)�����ӷ���ʽ����NO������ԭ��___________________________________��
(4)�ӻ�ѧ��Ӧ�������ȵĽǶȶ���ϵ�д��ڵķ�Ӧ���з�Ӧ��Fe2+��HNO3��Ӧ����Ӧ��Fe2+��NO��Ӧ�����û�ѧƽ���ƶ�ԭ��������Һ����ɫ��Ϊ��ɫ��ԭ��_____________________________��
����Ŀ�������£����ʵ���֮��Ϊ2��1��SO2��O2�Ļ���������ݻ�Ϊ2 L�ĺ����ܱ������з�����Ӧ��2SO2(g)��O2(g)![]() 2SO3(g)(����ӦΪ���ȷ�Ӧ)��n(SO2)��ʱ��仯��ϵ���±���
2SO3(g)(����ӦΪ���ȷ�Ӧ)��n(SO2)��ʱ��仯��ϵ���±���
ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
����˵����ȷ����( )
A. ��������������ܶȲ���ʱ���÷�Ӧ�ﵽƽ��״̬
B. �÷�Ӧ���е���3����ʱ���淴Ӧ����С������Ӧ����
C. �ӷ�Ӧ��ʼ���ﵽƽ�⣬��SO3��ʾ��ƽ����Ӧ����Ϊ0.01 mol/(L��min)
D. �����ڴﵽƽ��״̬ʱ��ѹǿ����ʼʱ��ѹǿ֮��Ϊ5��4