题目内容
【题目】磷酸铝(AlPO4)是一种用途广泛的材料,可在玻璃生产过程中充当助熔剂,作陶瓷或牙齿的黏合剂等。以磷硅渣[主要成分为Ca3(PO4)2、Al2O3、SiO2和V2O5等]为原料制备磷酸铝的工艺流程如图所示:

请回答下列问题:
(1)浸渣中含有SiO2,试写出SiO2的一种重要用途__;酸浸中磷元素主要转化为H3PO4,该反应的化学方程式为__。
(2)生石灰除了调节pH外,另一作用是__。
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为__。
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是__(填化学式)。
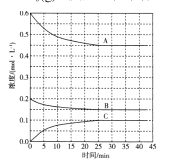
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量w%的影响如图所示:

则最优反应条件是__。
(6)在物质的量浓度分别为0.01mol·L-1的CaCl2和AlCl3的混合溶液中加入等体积的Na3PO4溶液,若A13+恰好沉淀完全,即溶液中c(A13+)=1.0×10-5mol·L-1,此时AlPO4沉淀中__(填“是”或“否”)混有Ca3(PO4)2。[已知AlPO4、Ca3(PO4)2的Ksp分别为6.3×10-19、2.0×10-29]
【答案】制备光导纤维 Ca3(PO4)2+3H2SO4=3CaSO4+2H3PO4 除去过量的硫酸根离子 V3O93﹣+3H2O3[VO3(OH)]2﹣+3H+ NaAlO2、Na3PO4 pH=12、温度为80℃、时间为1h 否
【解析】
磷硅渣的主要成分为Ca3(PO4)2、Al2O3、SiO2 和V2O5 等,加浓硫酸分离出滤渣为SiO2、CaSO4,酸浸液中加CaO可调节pH且除去过量硫酸根离子,滤渣1为CaSO4,滤液中钒元素以V3O93﹣形式存在,加NaOH分离出Na2[VO3(OH)],再加NaOH时粗磷酸铝溶解生成可溶性溶质为NaAlO2、Na3PO4,由图可知,pH=12、温度为80℃、时间为1h时碱浸时固相中P、Al 含量w%小,为最优反应条件,然后过滤分离出AlPO4,以此来解答。
(1)浸渣中含有SiO2,SiO2的重要用途为制备光导纤维、玻璃或水泥、硅等;酸浸中磷元素主要转化为H3PO4,该反应的化学方程式为Ca3(PO4)2+3H2SO4=3CaSO4+2H3PO4;
(2)生石灰除了调节pH 外,另一作用是除去过量的硫酸根离子;
(3)滤液中钒元素以V3O93﹣形式存在,V3O93﹣易水解为[VO3(OH)]2﹣,该水解反应的离子方程式为V3O93﹣+3H2O3[VO3(OH)]2﹣+3H+;
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是NaAlO2、Na3PO4;
(5)由图可知,pH=12、温度为80℃、时间为1h时碱浸时固相中P、Al 含量w%小,为最优反应条件;
(6)物质的量浓度分别为0.01 molL﹣1的CaCl2和AlCl3的混合溶液中加入等体积的Na3PO4 溶液,c(Ca2+)=0.01mol/L×![]() =0.005mol/L,c(Al3+)=1.0×10﹣5 molL﹣1,此时c(PO43﹣)=
=0.005mol/L,c(Al3+)=1.0×10﹣5 molL﹣1,此时c(PO43﹣)=![]() =6.3×10﹣14mol∥L,Qc[Ca3(PO4)2]=(0.005)3×(6.3×10﹣14)2=7.9×10﹣35<Ksp=2.0×10﹣29,没有Ca3(PO4)2沉淀。
=6.3×10﹣14mol∥L,Qc[Ca3(PO4)2]=(0.005)3×(6.3×10﹣14)2=7.9×10﹣35<Ksp=2.0×10﹣29,没有Ca3(PO4)2沉淀。