题目内容
19.关于反应2SO2+O2?催化剂△2SO3的说法正确的是( )| A. | 适宜条件下,SO2和O2可以完全转化为SO3 | |
| B. | 反应达到平衡后正逆反应的速率皆为零 | |
| C. | 若用18O2进行反应,达到平衡时二氧化硫中也会有18O | |
| D. | 工业合成SO3时,既要考虑反应速率也要考虑反应限度 |
分析 A、该反应为可逆反应,所以反应物不可能全部转化为生成物;
B、根据平衡状态的特征可知,平衡时是动态平衡,正逆反应速率相等但不等于零;
C、因为该反应为可逆反应,平衡时是动态平衡,据此判断;
D、在工业合成SO3时,因为要考虑生产效益,所以既要考虑反应速率又要考虑反应能达到的限度.
解答 解:A、该反应为可逆反应,所以反应物不可能全部转化为生成物,故A错误;
B、根据平衡状态的特征可知,反应处于平衡状态时,正逆反应速率相等但不等于零,故B错误;
C、因为该反应为可逆反应,平衡时是动态平衡,所以在SO2中也会含有18O,故C正确;
D、在工业合成SO3时,因为要考虑生产效益,所以既要考虑反应速率又要考虑反应能达到的限度,即反应物的转化率问题,故D正确;
故选CD.
点评 本题主要考查化学平衡的特征以及可逆反应在化学工工业生产的应用问题,中等难度,解题要注意化学原理与工业生产实际相结合.

练习册系列答案
相关题目
9.不法商贩为了使银耳增白,用硫磺(燃烧硫磺)对银耳进行熏制,这种银耳增白的方法是利用( )
| A. | S的漂白性 | B. | S的还原性 | C. | SO2的漂白性 | D. | SO2的还原性 |
10.工业上常用还原沉淀法处理含铬废水(Cr2O72-和CrO42-),其流程为:
CrO2−4(黄色)→H+①转化Cr2O2−7(橙色)→Fe2+②还原Cr3+→OH−③沉淀Cr(OH)3↓
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)?Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)•c3(OH-)=10-32
下列有关说法不正确的是( )
CrO2−4(黄色)→H+①转化Cr2O2−7(橙色)→Fe2+②还原Cr3+→OH−③沉淀Cr(OH)3↓
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)?Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)•c3(OH-)=10-32
下列有关说法不正确的是( )
| A. | 步骤①中当v正(CrO42-)=2v逆(Cr2O72-)时,说明反应:2CrO42-+2H+?Cr2O72-+H2O 达到平衡状态 | |
| B. | 若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色 | |
| C. | 步骤②中,若要还原1 mol Cr2O72-离子,需要12 mol (NH4)2Fe(SO4)2 | |
| D. | 步骤③中,当将溶液的pH 调节至5 时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+)≤10-5 mol/L时,可视作该离子沉淀完全) |
14.下列物质中含有碳碳双键的是( )
| A. | 乙烷 | B. | 乙炔 | C. | 乙烯 | D. | 苯 |
11.下列各组物质熔化或升华时,所克服的粒子间作用力属于同种类型的是( )
| A. | Na20和SiO2熔化 | B. | 冰和金刚石熔化 | ||
| C. | 氯化钠和蔗糖熔化 | D. | 碘和干冰升华 |
8.下列鉴别方法可行的是( )
| A. | 用氨水鉴别Al3+、Mg2+和Ag+ | |
| B. | 用盐酸、BaCl2溶液鉴别Cl-、SO42-和CO32- | |
| C. | 用溴水鉴别CH4和C2H4 | |
| D. | 用KMnO4酸性溶液鉴别CH3CH2OH和CH3CHO |
9.石墨晶体是层状结构,右图是其晶体结构的俯视图,则图中7个六元环完全占有的碳原子数是( )
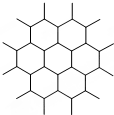

| A. | 10个 | B. | 14个 | C. | 18个 | D. | 24个 |
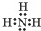 ;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.
;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.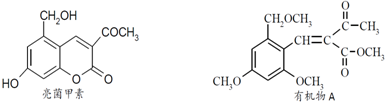
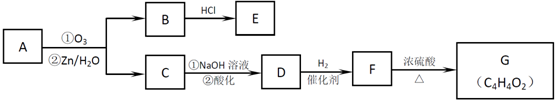
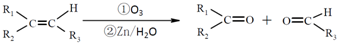
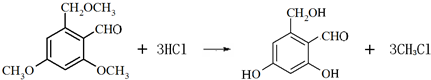 .
. .
.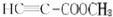 .
.