题目内容
5.配制一定体积、一定物质的量浓度的溶液,下列情况对实验结果产生偏高影响的是( )| A. | 定容时俯视观察液面 | |
| B. | 容量瓶中原有少量蒸馏水 | |
| C. | 溶解所用的烧杯、玻璃棒未洗涤 | |
| D. | 转移溶液时不慎将少量液体洒落在外 |
分析 根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:A、定容时俯视刻度线,会导致溶液体积偏小,则浓度偏大,故A正确;
B、只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,即容量瓶未干燥即用来配制溶液,对溶液浓度无影响,故B错误;
C、烧杯和玻璃棒未洗涤,会造成溶质的损失,则浓度偏低,故C错误;
D、移液时有溶液洒出,会导致溶质的损失,则浓度偏低,故D错误.
故选A.
点评 本题考查了一定物质的量浓度溶液的配制过程中的误差分析,属于基础型题目,难度不大,关键在于理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列操作或事实正确的是( )
| A. | 常温下,用pH试纸测得某新制氯水的pH值为9 | |
| B. | 用标准盐酸溶液滴定一定体积的待测NaOH溶液时,用石蕊做指示剂 | |
| C. | 用碱式滴定管量取高锰酸钾溶液5.10 mL | |
| D. | 用10 mL的量筒量取8.5 mL浓硫酸 |
20.下列反应的离子方程式书写正确的是( )
| A. | 过氧化钠和冷水反应:Na2O2+H2O═2Na++2OH-+H2↑ | |
| B. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
10.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 10g 46%的乙醇溶液所含氢原子数为1.2NA | |
| B. | 0.5 mol熔融的NaHSO4中含有的离子数目为1.5NA | |
| C. | 标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA | |
| D. | S2和S8的混合物共38.4g,其中所含硫原子数为1.4NA |
14.下列说法中,错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| D. | 能量变化是化学反应的基本特征之一 |
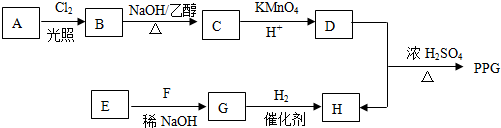
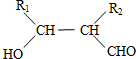
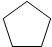 .
. .
.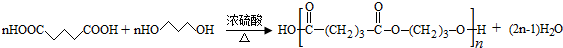 .
. (写构简式)
(写构简式)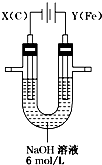 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,产率高,易于实验室制备.其原理如图所示,其总电解反应为:
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,产率高,易于实验室制备.其原理如图所示,其总电解反应为: .在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ClO-+H2↑.将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.
.在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ClO-+H2↑.将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.