题目内容
【题目】重铬酸钾是一种重要的化工原料,工业上由铬铁矿(主要成分为FeO·Cr2O3、SiO2等)制备,制备流程如图所示:
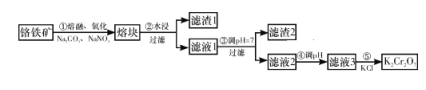
已知:
Ⅰ.步骤①的主要反应为2FeO·Cr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
Ⅱ.2CrO42-+2H+![]() Cr2O72-+H2O。
Cr2O72-+H2O。
下列说法正确的是( )
A. 步骤①熔融、氧化可以在陶瓷容器中进行
B. 步骤①中每生成44.8 L CO2共转移7 mol电子
C. 步骤④若调节滤液2的pH,使之变小,则有利于生成Cr2O72-
D. 步骤⑤生成K2Cr2O7晶体,说明该温度下K2Cr2O7的溶解度大于Na2Cr2O7
【答案】C
【解析】
铬铁矿的主要成分为FeO·Cr2O3、SiO2等,制备重铬酸钾,由制备流程可知,步骤①的主要反应为2FeO·Cr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2,Cr元素的化合价由+3价升高为+6价,Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+3价。步骤①中若使用陶瓷,二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,则使用铁坩埚,滤液2中含Na2CrO4,④中调节pH发生2CrO42-+2H+
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2,Cr元素的化合价由+3价升高为+6价,Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+3价。步骤①中若使用陶瓷,二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,则使用铁坩埚,滤液2中含Na2CrO4,④中调节pH发生2CrO42-+2H+![]() Cr2O72-+H2O,滤液3含Na2Cr2O7,由水中的溶解度:Na2Cr2O7>K 2Cr2O7,可知⑤中向Na2Cr2O7溶液中加入KCl固体后得到K 2Cr2O7,溶解度小的析出,以此来解答。
Cr2O72-+H2O,滤液3含Na2Cr2O7,由水中的溶解度:Na2Cr2O7>K 2Cr2O7,可知⑤中向Na2Cr2O7溶液中加入KCl固体后得到K 2Cr2O7,溶解度小的析出,以此来解答。
A.由上述分析可知,步骤①熔融、氧化不能使用陶瓷容器,原因是二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,故A错误;
B. 由上述分析可知步骤①的主要反应为2FeO·Cr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2,Cr元素的化合价由+3价升高为+6价,Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+3价,每生成2molCO2转移7mol电子,但没指明标况,故无法计算CO2的物质的量,故B错误;
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2,Cr元素的化合价由+3价升高为+6价,Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+3价,每生成2molCO2转移7mol电子,但没指明标况,故无法计算CO2的物质的量,故B错误;
C. 步骤④若调节滤液2的pH,发生2CrO42-+2H+![]() Cr2O72-+H2O,pH变小,平衡正向移动,则有利于生成Cr2O72-,故C正确;
Cr2O72-+H2O,pH变小,平衡正向移动,则有利于生成Cr2O72-,故C正确;
D. 向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体,说明步骤⑤发生Na 2Cr2O7+2KCl= K 2Cr2O7↓+2NaCl,说明该温度下K2Cr2O7的溶解度小于Na2Cr2O7,故D错误。
故答案选C。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案