题目内容
【题目】下列有关化学用语使用正确的是
A. 次氯酸的结构式:H—Cl—O B. 乙醇的结构简式: C2H6O
C. 硫离子的结构示意图:![]() D. 丙烷分子的球棍模型:
D. 丙烷分子的球棍模型:![]()
【答案】D
【解析】A.次氯酸分子中不存在氢氯键,其中心原子为氧原子;B.乙醇的的结构简式中要标出官能团;C.硫离子与硫原子的核电荷数相同,所以硫离子的核电荷数应该为16,不是18;D、注意区分球棍模型和比例模型。
A.次氯酸的电子式为:![]() ,将电子式中所有共用电子对换成短线,即为次氯酸的结构式,所以次氯酸的结构式为:H-O-Cl,选项A错误;B.乙醇的结构简式为C2H5OH, C2H6O为乙醇的分子式,选项B错误;C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示意图为:
,将电子式中所有共用电子对换成短线,即为次氯酸的结构式,所以次氯酸的结构式为:H-O-Cl,选项A错误;B.乙醇的结构简式为C2H5OH, C2H6O为乙醇的分子式,选项B错误;C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示意图为: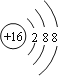 ,选项C错误;D、
,选项C错误;D、![]() 原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,选项D正确。答案选D。
原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,选项D正确。答案选D。

练习册系列答案
相关题目