题目内容
3.设NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 5.6 g 铁在足量氯气中燃烧,转移电子数为0.2 NA | |
| B. | 1mol H3O+所含的电子数为11NA | |
| C. | 71 g氯气与足量铁反应得到的电子数一定为2NA | |
| D. | 16 g O2和O3的混合气体中,含O2分子数为0.5NA |
分析 A、求出铁的物质的量,然后根据铁与氯气反应后变为+3价来分析;
B、H3O+为10电子微粒;
C、求出氯气的物质的量,然后根据氯气与铁反应后变为-1价来分析;
D、混合物中氧气的质量百分含量不明确.
解答 解:A、5.6g铁的物质的量为0.1mol,而铁与氯气反应后变为+3价,故0.1mol铁反应后转移0.3mol电子即0.3NA个,故A错误;
B、H3O+为10电子微粒,故1molH3O+含10mol电子即10NA个,故B错误;
C、71g氯气的物质的量为1mol,而氯气与铁反应后变为-1价,故1mol氯气与铁反应后得到2mol电子即2NA个,故C正确;
D、混合物中氧气的质量百分含量不明确,故含有的氧气分子个数不能计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
14.配制一定浓度的氯化钠溶液时,下列操作会使所配溶液浓度偏高的是( )
| A. | 溶液转移至容量瓶过程中不慎溅出 | |
| B. | 容量瓶中存在少量蒸馏水 | |
| C. | 溶液转移至容量瓶后,没有洗涤烧杯 | |
| D. | 定容时俯视刻度 |
18.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 强酸性溶液中:Mg2+、K+、SO42-、NO3- | |
| B. | 强碱性溶液中:Na+、Cu2+、H CO3-、NO3- | |
| C. | AgNO3 溶液中:H+、K+、SO42-、Cl- | |
| D. | Ba(NO3)2 溶液中:Mg2+、K+、SO42-、Cl- |
15.下列对“钾和钠性质相似”这个事实的解释最恰当的是( )
| A. | 它们都是金属元素 | B. | 它们的原子半径相差不大 | ||
| C. | 它们的最外层电子数相同 | D. | 它们的最高化合价相同 |
12.下列有关0.2mol•L-1 BaCl2溶液的说法正确的是( )
| A. | 1L溶液中Cl-离子浓度为0.2mol•L-1 | |
| B. | 1L溶液中Ba2+离子浓度为0.2mol•L-1 | |
| C. | 1L溶液中Cl-离子总数为0.2NA | |
| D. | 1L溶液中Ba2+和Cl-离子总数为0.6NA |
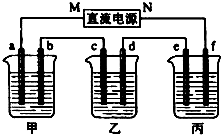 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放109g5.51%的NaOH溶液、足量的CuSO4溶液和200g10.00%的K2SO4溶液.电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放109g5.51%的NaOH溶液、足量的CuSO4溶液和200g10.00%的K2SO4溶液.电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: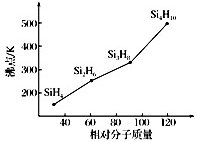 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
 D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质