题目内容
12.下列有关0.2mol•L-1 BaCl2溶液的说法正确的是( )| A. | 1L溶液中Cl-离子浓度为0.2mol•L-1 | |
| B. | 1L溶液中Ba2+离子浓度为0.2mol•L-1 | |
| C. | 1L溶液中Cl-离子总数为0.2NA | |
| D. | 1L溶液中Ba2+和Cl-离子总数为0.6NA |
分析 A、氯离子的浓度=氯化钡的物质的量浓度×一个化学式中氯离子的个数;
B、钡离子的浓度=氯化钡的物质的量浓度×一个化学式中钡离子的个数;
C、根据N=nNA=CVNA结合化学式计算氯离子的个数;
D、N=nNA=CVNA结合化学式计算离子的个数.
解答 解:A、0.2mol•L-1 BaCl2溶液中氯离子的物质的量浓度为0.4mol/L,与溶液的体积无关,故A错误;
B、0.2mol•L-1 BaCl2溶液中钡离子的物质的量浓度为0.2mol/L,与溶液的体积无关,故B正确;
C、N=nNA=cVNA=0.2mol•L-1×1L×2×NA=0.4NA,故C错误;
D、N=nNA=cVNA=0.2mol•L-1×1L×3×NA=0.5NA,故D正确.
故选BD.
点评 本题考查了物质的量浓度的有关计算,难度不大,注意溶液中不水解的离子的物质的量浓度与化学式和溶质的物质的量浓度有关,与溶液的体积无关

练习册系列答案
相关题目
2.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- | |
| B. | 0.1mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | 0.1mol•L-1的HCl溶液:Ca2+、Na+、ClO-、NO3- |
3.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 5.6 g 铁在足量氯气中燃烧,转移电子数为0.2 NA | |
| B. | 1mol H3O+所含的电子数为11NA | |
| C. | 71 g氯气与足量铁反应得到的电子数一定为2NA | |
| D. | 16 g O2和O3的混合气体中,含O2分子数为0.5NA |
20.反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加C的量 | B. | 将容器的体积缩小一半 | ||
| C. | 保持体积不变,充入H2O(g) | D. | 保持压强不变,充入N2 |
7.物质的量相同的碳酸钠和碳酸氢钠分别跟过量盐酸反应,下列说法正确的是( )
| A. | 碳酸钠放出CO2多 | B. | 碳酸氢钠放出CO2多 | ||
| C. | 碳酸钠消耗盐酸多 | D. | 碳酸氢钠消耗盐酸多 |
1. 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示,有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示,有关该物质的说法中正确的是( )
 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示,有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示,有关该物质的说法中正确的是( )| A. | 该物质遇FeCl3溶液呈紫色 | |
| B. | 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键 | |
| C. | 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol和7mol | |
| D. | 该分子中的所有碳原子不可能共平面 |
2.硫酸钙可用生产疏酸、漂白粉等一系列物质.下列说法正确的是( )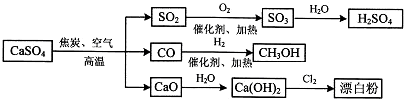

| A. | 由CO与H2合成CH3CH2OHO的反应中,原子利用率为100% | |
| B. | 向蔗糖中加入浓硫酸,蔗糖变黑同时产生刺激性气味的气体,说明浓硫酸具有脱水性和强氧化性 | |
| C. | 二氧化硫和漂白粉都能使品红溶液褪色,两者漂白性质相同 | |
| D. | 图中所有反应均为氧化还原反应 |
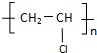 :
: