��Ŀ����
20��Ǧ�ĵ��ʡ������Ǧ�����ִ���ҵ��������Ҫ����;��1����ҵ����пұ�������е�Ǧ������������Ǧ����������[��֪Ǧ��������Ҫ�ɷ���PbO��Pb������������Ag��Zn��CaO��������������������ʣ�25��ʱ��Ksp��CaSO4��=5��10-5��Ksp��PbSO4��=1.6��10-8��]��
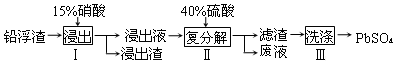
�����������У�����ʹ���������Ժ�������Ǧ���ʣ���Ŀ���Ƿ�ֹ���ܽ��������У���Һ�д��ڿ�ѭ�������ڵ����ʣ���������HNO3��
��д����������е���Ǧ��Ӧ�Ļ�ѧ����ʽ��3Pb+8HNO3=3Pb��NO3��2+2NO��+4H2O���������ﺬ�м�����CaSO4����ϴ�Ӽ����ʹ��c
a��ˮ b��10%���ᡢˮ c��Pb��NO3��2��Һ��ˮ
�۵���Һ��ij�ֽ�������Ũ��С��10-5mol•L-1ʱ������Ϊ�����Ӽ�ȫ������������Һ��c��Ca2+��=0.05mol•L-1�����ж�Ǧ�����Ƿ������ȫ��д����Ҫ�ļ�����̣�����������ȫ��
��2����֪Ǧ���γɶ�������������������PbO������������PbO2�����⣬Pb3O4��ǦԪ�ؼ�̬������Fe3O4�����ļ�̬��Pb3O4�������ᷢ����������ԭ��Ӧ����һ���κ�һ��Ǧ�������д����Ӧ�Ļ�ѧ����ʽPb3O4+4HNO3=PbO2+2Pb��NO3��2+2H2O��
��3��Pb��PbO2��PbSO4���ǹ���Ǧ���ص����ʣ�Ǧ���ط�ӦʽΪ��
Pb��s��+PbO2��s��+2H2SO4��aq��$?_{���}^{�ŵ�}$2PbSO4��s��+2H2O��l��
�ٳ��ʱ�����������ķ�Ӧ�ɱ�ʾΪPbSO4+2H2O-2e-=PbO2+SO42-+4H+��
�ڷŵ����ɵĹ���ḽ���ڵ缫���棬��������������������96gʱ�������ϵ�·��ת�Ƶĵ�����Ϊ3NA��
���� ��1��������Ǧ�����к���Ag���ʣ��ʲ�����Ag����ϡ���ᣬPb�Ļ�����ǿ��Ag����Pbʣ�������ֹAg�ܽ���ϡ���ᣬ���ڴ˷�Ӧ������NO���ʿ���ѭ���������
��ϡ����Ļ�ԭ����ΪNO��Pb��������������Ǧ������Ǧ������ˮ���ݴ˽��ѡȡ��ϴ���Լ���
�������ܶȻ��������㼴�ɣ�
��2��Pb3O4����дΪ��PbO•PbO2���ݴ���д����ʽ���ɣ�
��3��Ǧ���طŵ�ʱ��������Pbʧ���ӷ���������Ӧ������������Ǧ�õ��ӷ�����ԭ��Ӧ�����ʱ�����������缫��Ӧʽ�븺����������Ӧʽ�����෴��������PbO2��ΪPbSO4���������ӵ����൱�ڶ�����������������������ת�Ƶ��������Ĺ�ϵʽ����ת�Ƶ�������
��� �⣺��1����������Ҳ�������ᷴӦ������û��Ǧ���ã���Ǧ������ʣ��ʱ�����Ͳ����ܽ������У��ʽ��������躬��������Ǧ���ʣ���Һ�е���Ҫ�ɷ���HNO3��������ѭ�����ã��ʴ�Ϊ����ֹ���ܽ��������У�HNO3��
��ϡ���ỹԭ����ΪNO��Pb��ϡ���ᷴӦ��������Ǧ��NO��ˮ����ѧ��Ӧ����ʽΪ��3Pb+8HNO3=3Pb��NO3��2+2NO��+4H2O��������Pb��NO3��2��Һϴ�ӣ������ˮϴ�ӣ��������ȿɽ�CaSO4ת��ΪPbSO4�ﵽ��ȥ�ӻ���Ŀ�ģ��ֿ����ǦԪ�ص������ʣ��ʴ�Ϊ��3Pb+8HNO3=3Pb��NO3��2+2NO��+4H2O��c��
��Ksp��CaSO4��=5��10-5=c��Ca2+����c��SO42-��=0.05mol•L-1��c��SO42-������c��SO42-��=$\frac{5��1{0}^{-5}}{0.05}$=10-3����ʱc��Pb2+��=$\frac{1.6��1{0}^{-8}}{1{0}^{-3}}$=1.6��10-5mol/L�����ڸ�û���γ�CaSO4����������Һ��c��SO42-����1��10-3mol•L-1��c��Pb2+����1.6��10-5mol/L��1��10-5mol/L���ʳ�������ȫ���ʴ�Ϊ����������ȫ��
��2������Ŀ��Ϣ֪Pb3O4��Ǧ�Ļ��ϼ�Ϊ+2��+4���ּ�̬���൱��2PbO•PbO2������PbO2������������������������ᷴӦ��PbO�Ǽ���������������ᷢ����������ԭ��Ӧ������Pb��NO3��2���ɴ˿�д����Ӧ�Ļ�ѧ����ʽ��Pb3O4+4HNO3=PbO2+2Pb��NO3��2+2H2O���ʴ�Ϊ��Pb3O4+4HNO3=PbO2+2Pb��NO3��2+2H2O��
��3����Ǧ���ع���ʱ��������ⷴӦ��Pb-2e-+SO42-=PbSO4 �������缫��Ӧ��PbO2+2e-+4H++2SO42-=PbSO4+2H2O�����ʱ������Ӧʽ��������Ӧ�����෴����������ӦʽΪPbSO4+2H2O-2e-�TPbO2+4H++SO42-�����ʴ�Ϊ��PbSO4+2H2O-2e-�TPbO2+4H++SO42-��
��������PbO2��ΪPbSO4���������ӵ����൱�ڶ���������PbO2+2e-+4H++SO42-=PbSO4+2H2O֪��ת�Ƶ�����=$\frac{96g}{64g/mol}$��2��NA/mol=3NA���ʴ�Ϊ��3��
���� ���⿼����Ǧ���ص�ԭ���ȣ��漰�ŵ���̺ͳ����̣��ؼ�ץס�ŵ�ʱ����ԭ��صĹ���ԭ�������ʱ�ǵ��صĹ���ԭ������Ŀ�Ѷ��еȣ�

| A�� | Fe | B�� | Mg | C�� | P | D�� | Na |
| A�� | �Ҵ������ᶼ�������Ʒ�Ӧ�������� | |
| B�� | ��֬�����ۡ���ά�ض�������Ȼ�߷��ӻ����� | |
| C�� | �ױ�����ϩ��������ˮ������ѧ��Ӧ�����ˮ��ɫ | |
| D�� | ��������Һ����CuSO4��Һ����������һ�������ڵ����ʵ����� |

| A�� | ��ͼ����Ϣ��֪HAΪǿ�ᣬN���ʾ���ǡ���к� | |
| B�� | �����£�һ��Ũ�ȵ�MAϡ��Һ��pH��7 | |
| C�� | K������Ӧ����Һ������Ũ�ȵĴ�С��ϵ��c��M+����c��OH-����c��A-����c��H+�� | |
| D�� | K���Ӧ����Һ�У���Һ��pH��13��c��HA��+c��A-��=0.25mol•L-1 |
| A�� | ���̵����кͼ��Է�ˮ | B�� | �ظ�������ھƼݼ�� | ||
| C�� | �ñ��������ȩ��֬ | D�� | �����ӹ�ǰ��������ϴ |
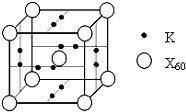 ��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������p�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�������ش��������⣺
��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������p�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E�ĵ����dz�����Ψһ��Һ̬�ķǽ�������ش��������⣺ ij�о���ѧϰС��Ϊ̽��п�����ᷴӦ��ȡͬ������ͬ�����пƬ��ͬŨ��������������ƽ��ʵ�飺
ij�о���ѧϰС��Ϊ̽��п�����ᷴӦ��ȡͬ������ͬ�����пƬ��ͬŨ��������������ƽ��ʵ�飺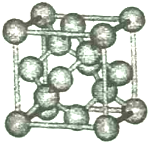 2014��12��6���й��������������ձ�������ѧ��ѧ��ȷ���������·��ֵľ��и߶Ȼ��ԵĹ軯��SiC2N��SiC3N���ӣ������о�������������ѧ�����Ǽʽ�����Ѱ����ط��ӣ��ش��������⣺
2014��12��6���й��������������ձ�������ѧ��ѧ��ȷ���������·��ֵľ��и߶Ȼ��ԵĹ軯��SiC2N��SiC3N���ӣ������о�������������ѧ�����Ǽʽ�����Ѱ����ط��ӣ��ش��������⣺
 ��
�� ������һ�֣���
������һ�֣��� ���ĺϳ�·�ߣ�
���ĺϳ�·�ߣ�