题目内容
18.下列关于有机化合物的说法中,正确的是( )| A. | 乙醇、乙酸都可以与钠反应生成氢气 | |
| B. | 油脂、淀粉、纤维素都属于天然高分子化合物 | |
| C. | 甲苯和乙烯都可与溴水发生化学反应造成溴水褪色 | |
| D. | 蛋白质溶液加入CuSO4溶液会析出,这一过程属于蛋白质的盐析 |
分析 A.乙醇中含有羟基,乙酸中含有羧基,均能与钠反应生成氢气;
B.相对分子质量在10000以上的物质属于高分子化合物;
C.甲苯分子中不存在碳碳双键或碳碳三键,不能使溴水褪色;
D.蛋白质溶液加入CuSO4溶液会析出,该过程为蛋白质的变性.
解答 解:A.钠化学性质比较活泼,乙醇中含有羟基,乙酸中含有羧基,所以二者均能与钠反应生成氢气,故A正确;
B.蛋白质、纤维素、淀粉属于高分子化合物,油脂相对分子质量较小,不属于高分子化合物,故B错误;
C.乙烯分子中含有碳碳双键,能够使溴水褪色,而甲苯不与溴水反应,不能使溴水褪色,故C错误;
D.蛋白质溶液加入CuSO4溶液会析出,这一过程为化学变化,属于蛋白质的变性,不是盐析,故D错误;
故选A.
点评 本题考查了有机物结构与性质、高分子化合物的判断,题目难度中等,注意掌握常见有机物结构与性质,明确蛋白质的盐析与变性的区别,B为易错点,注意明确高分子化合物的概念及判断方法.

练习册系列答案
相关题目
8.能证明苯酚具有酸性的方法是( )
①苯酚溶液加热变澄清 ②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水 ③苯酚可与FeCl3反应 ④在苯酚溶液中加入浓溴水产生白色沉淀 ⑤苯酚能与Na2CO3溶液反应.
①苯酚溶液加热变澄清 ②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水 ③苯酚可与FeCl3反应 ④在苯酚溶液中加入浓溴水产生白色沉淀 ⑤苯酚能与Na2CO3溶液反应.
| A. | ③④ | B. | ①②⑤ | C. | ②⑤ | D. | ③④⑤ |
6.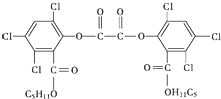 “魔棒”常被用于晚会现场气氛的渲染.“魔棒”发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列说法中正确的是( )
“魔棒”常被用于晚会现场气氛的渲染.“魔棒”发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列说法中正确的是( )
 “魔棒”常被用于晚会现场气氛的渲染.“魔棒”发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列说法中正确的是( )
“魔棒”常被用于晚会现场气氛的渲染.“魔棒”发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列说法中正确的是( )| A. | CPPO难溶于水 | |
| B. | CPPO属于芳香烃也属于高分子化合物 | |
| C. | 1 mol CPPO与氢气完全反应,需要10 mol H2 | |
| D. | 1 mol CPPO与NaOH稀溶液反应(不考虑苯环上氯原子水解),最多消耗4 mol NaOH |
13.以下反应中,Q1>Q2的是( )
| A. | S(s)+O2(g)→SO2(g)+Q1kJ;S(g)+O2(g)→SO2(g)+Q2kJ | |
| B. | H2(g)+$\frac{1}{2}$O2(g)→H2O(l)+Q1kJ;H2(g)+$\frac{1}{2}$O2(g)→H2O(g)+Q2kJ | |
| C. | NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)+Q1kJ NaOH(aq)+HAc(aq)→NaAc(aq)+H2O(l)+Q2kJ | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1kJ,H2(g)+I2(g)→2HI(g)+Q2kJ |
3.反应2C+CO2(g)?2CO(g)达到化学平衡后,保持其他条件不变,移走少量CO,达到新的平衡后,下列选项中,增大的是( )
| A. | CO2和CO浓度比 | B. | 混合气体的密度 | C. | 转化率 | D. | CO 的体积分数 |
3.化学镀是指使用合适的还原剂,使镀液中的金属离子还原成金属而沉积在镀件表面上的一种镀覆工艺.化学镀广泛用作金属、塑料、玻璃、陶瓷等许多材料的装饰和防护.在ABS工程塑料表面进行化学镀镍的流程如下:

回答下列问题:
(1)化学镀与电镀比较,优点之一是不需通电.
(2)镀件表面用热碱液清洗的作用是除去镀件表面油污,镀件表面粗化的目的是增强亲水性及增大接触面积.
(3)镀件浸入AgNO3溶液后,镀件表面吸附的SnCl2将AgNO3还原生成有催化活性的金属银,反应的化学方程式是2SnCl2+4AgNO3═4Ag+SnCl4+Sn(NO3)4.
(4)镀镍时,镀液中的Ni2+与H2PO2-在催化表面上反应沉积镍,同时生成中强酸H3PO3及与金属镍物质的量相等的氢气,该反应的离子方程式是2H2O+Ni2++2H2PO2-=Ni++H2↑+2H3PO3.
(5)化学镀某种金属时,反应时间与镀层厚度的实验数据记录如表所示:
由此推断,镀层厚度y与反应时间t的关系式为y=at1/2;欲使镀层厚度为6anm,需要的反应时间为36s.
(6)化学镀镍废液中含有Ni 2+等污染物,需转化为沉淀除去.已知25℃,Ksp[Ni(OH)2]=2.0×10-15.若加入碱后使废液的pH=10,则处理后的废液中镍元素的含量为1.2×10-2mg•L-1.

回答下列问题:
(1)化学镀与电镀比较,优点之一是不需通电.
(2)镀件表面用热碱液清洗的作用是除去镀件表面油污,镀件表面粗化的目的是增强亲水性及增大接触面积.
(3)镀件浸入AgNO3溶液后,镀件表面吸附的SnCl2将AgNO3还原生成有催化活性的金属银,反应的化学方程式是2SnCl2+4AgNO3═4Ag+SnCl4+Sn(NO3)4.
(4)镀镍时,镀液中的Ni2+与H2PO2-在催化表面上反应沉积镍,同时生成中强酸H3PO3及与金属镍物质的量相等的氢气,该反应的离子方程式是2H2O+Ni2++2H2PO2-=Ni++H2↑+2H3PO3.
(5)化学镀某种金属时,反应时间与镀层厚度的实验数据记录如表所示:
| 反应时间t/s | 1 | 4 | 9 | 16 |
| 镀层厚度y/nm | a | 2a | 3a | 4a |
(6)化学镀镍废液中含有Ni 2+等污染物,需转化为沉淀除去.已知25℃,Ksp[Ni(OH)2]=2.0×10-15.若加入碱后使废液的pH=10,则处理后的废液中镍元素的含量为1.2×10-2mg•L-1.
1.下列相关反应的离子方程式书写正确的是( )
| A. | 将钠粒投入CuSO4溶液中:2Na+Cu2+=Cu+2Na+ | |
| B. | 将NaHSO4溶液滴加到含有酚酞的Ba(OH)2溶液中,溶液由红色变成无色:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 将少量醋酸加入到NaAlO2溶液中:CH3COOH+AlO2-+H2O=CH3COO-+Al(OH)3↓ | |
| D. | 硫化钠溶液中加入少量的氯化铁溶液:S2-+2Fe3+=2Fe2++S↓ |