题目内容
10.某烃能使KMnO4溶液褪色,但不能使溴水褪色,其分子式为C8H10,该烃的一氯代物有三种(含侧链取代物),该烃的结构简式是 ;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为
;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为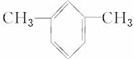 或
或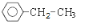 .
.
分析 根据分子式确定分子的不饱和度,不能使溴水因反应而褪色,说明不含双键,故为苯环,能使酸性KMnO4溶液褪色的芳香烃中,和苯环碳原子相连的碳上必须有氢原子;苯环上的一氯代物只有一种说明苯环上只有一种类型的氢原子.
解答 解:C8H10不能使溴水因反应褪色,说明结构中不含双键或三键,能使酸性高锰酸钾溶液褪色,说明是带侧链的取代苯,A可能为乙苯、邻二甲苯、间二甲苯、对二甲苯共4种,其中乙苯有4种H,故一氯代物有4种,邻二甲苯有3种H,故一氯代物有3种,间二甲苯有4种H,故一氯代物有4种,对二甲苯有2种H,故一氯代物有2种,符合题意的是邻二甲苯,结构简式为: ,若烃A分子中含苯环,且苯环上的3氯代物有3种的结构有:间二甲苯和乙苯2种,结构简式为:
,若烃A分子中含苯环,且苯环上的3氯代物有3种的结构有:间二甲苯和乙苯2种,结构简式为: 和
和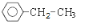 ,故答案为:
,故答案为: ;
;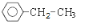 .
.
点评 本题考查有机物分子式确定的题目,有机物的结构与性质,注意把握有机物中的官能团及性质,题目难度中等.

练习册系列答案
相关题目
19.下列每组物质发生状态变化所克服的粒子间的相互作用属于同类型的是( )
| A. | 食盐和氯化氢溶于水 | B. | 钠和硫熔化 | ||
| C. | 碘和干冰升华 | D. | 二氧化硅和氧化钠熔化 |
1.“北大富硒康”中含有微量元素硒(Se),对人体有保健作用.已知硒为第4周期ⅥA族元素,根据它在周期表中的位置推测硒不可能具有的性质为( )
| A. | 硒化氢不稳定 | |
| B. | 硒化氢的水溶液显弱酸性 | |
| C. | 得电子能力强于硫 | |
| D. | 其最高价氧化物的水化物酸性强于砷弱于溴 |
18.有一混合溶液中含有以下离子中的若干:K+、NH4+、Cl-、HCO3-、SO32-、SO42-、Ag+.现取等体积的两份溶液进行如下实验:
(1)第一份加入足量的NaOH溶液,无沉淀;加热,收集到标准状况下的气体336mL.
(2)第二份加入足量的用盐酸酸化的BaCl2溶液,产生2.33g白色沉淀,同时收集到标准状况下的气体336mL,该气体能使品红溶液褪色.
根据上述实验,下列推断正确的是( )
(1)第一份加入足量的NaOH溶液,无沉淀;加热,收集到标准状况下的气体336mL.
(2)第二份加入足量的用盐酸酸化的BaCl2溶液,产生2.33g白色沉淀,同时收集到标准状况下的气体336mL,该气体能使品红溶液褪色.
根据上述实验,下列推断正确的是( )
| A. | K+一定存在 | |
| B. | Ag+和Cl-一定不存在 | |
| C. | HCO3-一定不存在 | |
| D. | 混合溶液中一定有0.015 mol SO32- |
15.下列说法中,正确的是( )
| A. | 任何溶液中,c(H+)×c(OH-)=1.0×10-14 | |
| B. | pH=0的溶液呈中性 | |
| C. | 酸性溶液中,c(H+)越大,酸性越强 | |
| D. | 酸性溶液中没有OH-,碱性溶液里没有H+ |
2.下列有关实验的说法正确的是( )
| A. | CH2=CH-CHO能使酸性高锰酸钾溶液褪色,证明该分子中一定含有碳碳双键 | |
| B. | 现向K2Cr2O7溶液中加入少量氢氧化钠,溶液变为黄色,证明溶液中存在着平衡:Cr2O72-+H2O?2CrO42-+2H+ | |
| C. | 用相互滴加的方法不能鉴别NaCl、AlCl3、Na2CO3、NaHSO4四种无色溶液 | |
| D. | SO2通入Ba(NO3)2溶液中出现白色沉淀,证明BaSO3不溶于水 |
19.已知:I2+2S2O32-═S4O62-+2I-,相关物质的溶度积常数见下表:
(1)常温下,某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入Cu(OH)2、CuO、CuCO3或Cu2(OH)2CO3,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,而是生成Cu(OH)Cl,写出相关的化学反应方程式:CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)Cl+HCl↑+H2O.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥HCl气流中加热制得.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀.过滤后,用0.100 0mol•L-1 Na2S2O3标准溶液滴定所得滤液,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉作滴定指示剂,滴定终点的现象是蓝色变为无色,且在半分钟内无变化.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95.0%.
20.氢原子的电子云图中的小黑点表示的意义是( )
| A. | 一个小黑点表示一个电子 | B. | 表示电子运动的轨迹 | ||
| C. | 电子在核外空间出现机会的多少 | D. | 黑点的多少表示电子个数的多少 |