题目内容
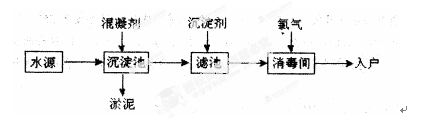
(15分)雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O3和NH4NO3产品的流程图如下(Ce为铈元素):
⑴装置Ⅰ中的主要离子方程式为 。3
⑵含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。

①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
⑶写出装置Ⅱ中,酸性条件下的离子方程式 。
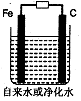
⑷装置Ⅲ还可以使Ce4+再生,其原理如下图所示。
①生成Ce4+从电解槽的 (填字母序号)口流出。②写出与阴极的反应式 。
⑸已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示, 计算结果保留整数)
(1) SO2+OH-=HSO3-;
(2) ①c(Na+)﹥c(SO32-)﹥c(HSO3-)﹥c(OH-)﹥c(H+) ;② HSO3-在溶液中存在电离平衡:HSO3- SO32-+ H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大
SO32-+ H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大
(3) NO+2H2O+3Ce4+=3Ce3++NO3-+4H+;NO+H2O+Ce4+=Ce3++NO2-+2H+
(4) ①a ; ②2HSO3-+4H++4e-=S2O32-+3H2O
(5)243a (242a、244a、5600a/23都给分)
解析试题分析:⑴在置Ⅰ中SO2与NaOH溶液发生反应,离子方程式是SO2+OH-=HSO3-;(2)①溶液的pH=8时,溶液中含有的物质是Na2SO3和NaHSO3.根据物料守恒可得c(Na+)=(SO32-)+(HSO3-)+(H2O3);所以c(Na+)最大。知c(SO32-)﹥c(HSO3-)由于溶液显碱性,所以c(OH-)﹥c(H+);因为盐是强电解质,盐水解的程度是微弱的,所以c(HSO3-)﹥c(OH-)。故溶液中的离子浓度关系为:c(Na+)﹥c(SO32-)﹥c(HSO3-)﹥c(OH-)﹥c(H+);②NaHSO3溶液的pH=5,说明在溶液中NaHSO3的电离作用大于水解作用,当向其中加入CaCl2溶液时,会发生反应:Ca2++SO32-=CaSO3↓,这样就破坏了溶液中HSO3-在溶液中存在电离平衡:HSO3- SO32-+ H+,使平衡正向移动,进行电离产生大量的H+;c(H+)增大,因此溶液的pH减小。pH降为2。⑶在装置Ⅱ中,在酸性条件下根据流程示意图可得反应的离子方程式是NO+2H2O+3Ce4+=3Ce3++NO3-+4H+;NO+H2O+ Ce4+=Ce3++NO2-+2H+;⑷在装置Ⅲ还可以使Ce4+再生,①由于Ce3+→Ce4+,化合价升高,失去电子,所以生成Ce4+从电解槽的阳极a流出;②在阴极发生的电极的反应式是2HSO3-+4H++4e-=S2O32-+3H2O。⑸由于NO2-的浓度为a g·L-1,所以1 m3该溶液中的NO2-的量为a g·L-1×1000L=1000ag.物质的量为1000ag÷46g/mol;每1mol的NO2-完全转化为NH4NO3,失去电子2mol.所以转移电子的物质的量为1000ag÷46g/mol×2=(1000a÷23)mol,每一mol的氧气反应转移电子4mol,所以消耗氧气的物质的量为(1000a÷23)mol÷4=(250a÷23)mol,需至少向装置Ⅳ中通入标准状况下的O2的体积是(250a÷23)mol×22.4L/mol=5600a/23L="243." 5aL。
SO32-+ H+,使平衡正向移动,进行电离产生大量的H+;c(H+)增大,因此溶液的pH减小。pH降为2。⑶在装置Ⅱ中,在酸性条件下根据流程示意图可得反应的离子方程式是NO+2H2O+3Ce4+=3Ce3++NO3-+4H+;NO+H2O+ Ce4+=Ce3++NO2-+2H+;⑷在装置Ⅲ还可以使Ce4+再生,①由于Ce3+→Ce4+,化合价升高,失去电子,所以生成Ce4+从电解槽的阳极a流出;②在阴极发生的电极的反应式是2HSO3-+4H++4e-=S2O32-+3H2O。⑸由于NO2-的浓度为a g·L-1,所以1 m3该溶液中的NO2-的量为a g·L-1×1000L=1000ag.物质的量为1000ag÷46g/mol;每1mol的NO2-完全转化为NH4NO3,失去电子2mol.所以转移电子的物质的量为1000ag÷46g/mol×2=(1000a÷23)mol,每一mol的氧气反应转移电子4mol,所以消耗氧气的物质的量为(1000a÷23)mol÷4=(250a÷23)mol,需至少向装置Ⅳ中通入标准状况下的O2的体积是(250a÷23)mol×22.4L/mol=5600a/23L="243." 5aL。
考查:离子方程式的书写、离子浓度的比较、电解原理及应用、氧化还原反应的有关计算的知识。

(16分)火力发电在我国的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题,直接排放含SO2的烟气会形成酸雨,危害环境。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: 。
(2)工业上用Na2SO3溶液吸收烟气中的SO2。将烟气通入1.0 mol·L-1的Na2SO3溶液,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂。
① 此时溶液中c(SO32–)的浓度是0.2 mol·L-1,则溶液中c(HSO3–)是_______mol?L-1。
② 向pH约为6的吸收剂中通入足量的O2,可将其中的NaHSO3转化为两种物质,反应的化学方程式是 。
③ 某研究小组为探究提高含硫烟气中SO2的
吸收效率的措施,模拟实验吸收含硫烟气,实验结果如图所示。则: ,
有利于提高SO2的吸收效率。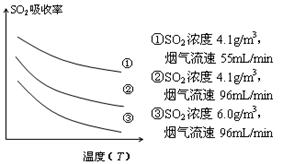
(3)工厂仓库存放的Na2SO3药品已部分被空气
氧化,该化学小组想用已知浓度的酸性KMnO4
溶液来确定其含量,具体步骤如下:
步骤i 称取样品1.000 g。
步骤ii 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤iii 移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01000 mol·L-1 KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
① 写出步骤iii所发生反应的离子方程式___________________________________;
② 在配制0.01000 mol·L-1 KMnO4溶液时若仰视定容,则最终测得药品中Na2SO3的含量________(填“偏大”、“偏小”或“无影响”)。
③ 某同学设计用下列仪器进行滴定实验(夹持部分略去),最合理的组合是_ (填字母)。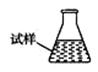
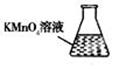

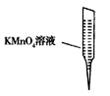
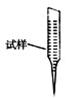
A B C D E
④ 滴定结果如下表所示:
| 滴定次数 | 待测溶液 的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
实验室用Na2SO3固体与70%的硫酸反应制取SO2气体时,可用FeC13溶液吸收多余的SO2气体。
(1)写出SO2与FeC13溶液反应的离子方程式: 。
(2)FeC13溶液吸收SO2气体一段时间后,吸收液中一定存在的离子有:H+、Fe2+、C1—、SO42-。某同学认为还可能存在其他离子,并提出假设进行实验探究。
①提出合理假设:
假设1:还存在HSO3-、SO32-
假设2:还存在Fe3+
假设3:HSO3-、SO32-、Fe3+都不存在
②设计实验方案
| 实验步骤 | 现象和结论 |
| 步骤1:取少量吸收液于试管,滴加稀硫酸酸化,然后再滴入几滴 溶液。 | 现象: 结论:假设1不成立。 |
| 步骤2: | 现象: 结论:假设2成立。 |
(3)测定空气中SO2含量的方法是:把500L含SO2气体的空气通入20mL含0.00015molKMnO4的溶液中,充分反应后,再用0.02000mol/L的KI溶液滴定过量的KMnO4,消耗KI 溶液25.00mL,则空气中的SO2含量为 mg/L。
(5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+,10I—+2MnO4-+16H+=2Mn2++5I2+8H2O)
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
| A.5.76 | B.2.88 | C.1.44 | D.4.32 |
将1.52 g的铜镁合金完全溶解于50mL14.0 mol/L的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加人1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
| A.若该浓硝酸的密度为1.40g/mL则该浓硝酸的溶质质量分数为63% |
| B.该合金中铜与镁的物质的最之比是2:1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加人NaOH溶液的体积是620 mL |
把含有FeBr2、FeI2各a mol的稀溶液两份,分别通入一定量的Cl2,第一份溶液中有一半的I― 被氧化成I2,第二份溶液中有一半的Br― 被氧化成Br2,两份通入Cl2的物质的量之比
| A.1:1 | B.1:2 | C.1:3 | D.1:5 |
在某100mL混合酸中,HNO3物质的量浓度为0.4mol.L-1,H2SO4物质的量浓度为0.2mol.L-1。向其中加入足量的铜粉,待充分反应后,溶液中Cu2+物质的量浓度为
| A.0.3mol.L-1 | B.0.225mol.L-1 | C.0.15mol.L-1 | D.无法计算 |