题目内容
水是生命之源,水处理工艺在生产生活中占有重要地位。自来水生产的流程示意图如下。(净水剂亦称混凝剂,常用的净水剂有聚合氯化铝、碱式氯化铝、硫酸亚铁、聚丙烯酰胺、聚合氯化铝铁、三氯化铁、聚合硫酸铁等)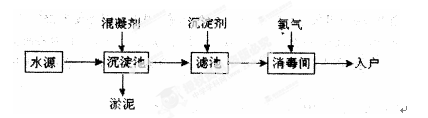
(1)FeSO4·7H2O是常用的混凝剂,它在水中最终生成 沉淀。
(2)[A12(OH)nClm]是一种无机高分子的高价聚合电解质混凝剂,可视为介于三氯化铝和氢氧化铝之间的一种中间水解产物,则m与n之间的关系 ;
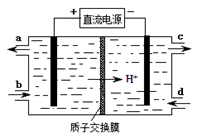
(3)推销净水器的商人用自来水做电解实验,装置如图。一段时间后,两极间产生白色沉淀,并很快变成红褐色,然后用净水器净化后的水做电解实验;两极上只有气体产生,水中并无沉淀,以此来说明自来水很“脏”。则沉淀变成红褐色时所发生的化学反应方程式为: 。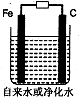
(4)MnSO4是水质检测中的一种常用试剂
①MnSO4和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸盐及另外一种产物,写出并配平上述反应的化学方程式: 。
②水中的溶解氧测定过程为:取水样,迅速加入MnSO4和KOH混合液,再加入KI溶液,立即塞好塞子,振荡使完全反应(反应为:Mn2++O2+H2O→MnOOH,未配平)。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。则该离子反应方程式: 。用Na2S2O3溶液滴定生成的碘,根据消耗溶液的体积可计算出水中溶解氧的量。
(1)Fe(OH)3
(2)m+n=6
(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(4)①2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,(Ag+催化剂)
②6H++2MnOOH+2I-=I2+2Mn2++4H2O
解析试题分析:
(1)FeSO4·7H2O溶于水,水解之后生成Fe(OH)2,继续被氧化成Fe(OH)3胶体,Fe(OH)3胶体有很强的吸附能力,将水中的悬浮颗粒物吸附并沉降下来,所以最终生成Fe(OH)3沉淀。
(2)由[A12(OH)nClm],根据化合价整体为0,因此m+n=6。
(3)铁在阳极放电,电极反应为:Fe-2e-=Fe2+,之后Fe2+ + 2OH- =Fe(OH)2↓,Fe(OH)2易被氧化,4Fe(OH)2 +O2+2H2O=4Fe(OH)3↓白色沉淀变成红褐色。
(4)①陌生情景下氧化还原反应方程式的书写步骤是:先写骨架(氧化剂、还原剂、氧化产物、还原产物),再根据电子守恒把骨架配平,最后根据原子守恒在方程式的两边在“H2O”上做文章。根据题意,硫酸锰被氧化成高锰酸钾,则过硫酸钾被还原成硫酸盐(硫酸钾),所以骨架为硫酸锰、过硫酸钾、高锰酸钾、硫酸钾,根据电子守恒把骨架配平,再根据原子守恒,方程式的左边有12个硫原子,右边只有4个硫原子,所以右边还缺8个硫原子,同时化合价应该是+6价,而钾原子已经守恒,所以只能是硫酸,如果在右边添加8H2SO4 ,再根据氢原子或者氧原子守恒,在方程式的左边补充“8H2O”。 ②取水样,迅速加入MnSO4和KOH混合液,再加入KI溶液,发生题干中的反应,即Mn2+被氧化成MnOOH,加入硫酸后,I-在酸性条件下被MnOOH氧化成I2,这也是一个氧化还原反应,书写思路同上,先写骨架并配平,再根据电荷守恒和原子守恒,在左边补充H+,在右边补充“H2O”即可。
考点:本题考查水处理工艺在生产生活中的应用。结合了胶体、电化学、氧化还原反应离子方程式的书写。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案KMnO4是一种重要的氧化剂。
(1)①在酸性条件下KMnO4的氧化性会增强。用来酸化KMnO4溶液的最佳试剂是 。
a.硝酸 b.硫酸 c.盐酸
②将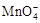 氧化C2O42?的离子方程式补充完整:
氧化C2O42?的离子方程式补充完整:
□MnO4? +□C2O42?+□ ==□Mn2+ +□CO2↑+□ 。
(2)某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100 mL 0.0400 mol·L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是 。
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60 s |
| 褪色后,再滴入第2滴 | 15 s |
| 褪色后,再滴入第3滴 | 3 s |
| 褪色后,再滴入第4滴 | 1 s |
请分析KMnO4溶液褪色时间变化的可能原因 。
③用配制好的0.040 0 mol·L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度。每次准确量取25.00 mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定。滴定三次分别消耗的KMnO4溶液的体积是20.00 mL、19.80 mL、20.20 mL,则KMnO4溶液的浓度为 。
宋代著名法医学家宋慈 的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2="==2" Ag2S +2H2O,其中H2S是
| A.氧化剂 | B.还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |
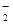 、MnO
、MnO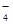 、CO
、CO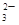 、SO
、SO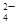 中的若干种离子组成,取溶液进行右图实验:
中的若干种离子组成,取溶液进行右图实验: