题目内容
【题目】用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 24.60 |
回答下列问题:
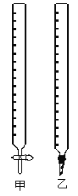
(1)如图中甲为___________滴定管,乙为_________ 滴定管(填“酸式”或“碱式 ”)
(2)实验中,需要润洗的仪器是:________________________
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是________________________________________
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果____________(填“偏高”“偏低”“不变”,下同);若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果___________。
(5) 未知浓度的NaOH溶液的物质的量浓度为_____________mol/l。
【答案】酸式 碱式 (酸、碱式)滴定管 红色褪去,半分钟不再出现红色 偏高 偏低 0.1288
【解析】
(1)根据仪器的结构来分析;
(2)酸、碱式滴定管洗涤后附着的水会稀释溶液,影响滴定结果;
(3)依据溶液的酸碱性来选择指示剂,根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(4)根据c(待测)=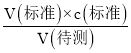 来判断;
来判断;
(5)先根据数据的有效性,然后求出平均消耗V(HCl),然后计算即可。
(1)甲滴定管的下端是玻璃活塞,所以仪器的名称为酸式滴定管,乙滴定管的下方是橡胶管,故名称为碱式滴定管;
(2)酸、碱式滴定管洗涤后附着的水会稀释溶液,影响滴定结果,故酸、碱式滴定管在盛装溶液时均先用所盛溶液润洗;
(3)滴定时用酚酞做指示剂,滴定达到终点的现象是:酚酞的红色褪去且半分钟不再出现红色;
(4)取标准液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,标准液的物质的量偏小,导致标准液的体积偏大,故根据c(待测)=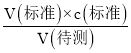 分析,C(待测)偏高;标准液读数时,若滴定前仰视,滴定后俯视,导致标准液的体积偏小,根据c(待测)=
分析,C(待测)偏高;标准液读数时,若滴定前仰视,滴定后俯视,导致标准液的体积偏小,根据c(待测)=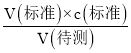 分析,C(待测)偏低;
分析,C(待测)偏低;
(5)依据数据可知,舍去差距较大的22.60mL,故V(标准)=![]() =24.40mL,c(待测)=
=24.40mL,c(待测)=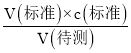 =
=![]() =0.1288mol/L。
=0.1288mol/L。

 通城学典默写能手系列答案
通城学典默写能手系列答案【题目】下列有关实验现象和解释或结论都正确的是()
选项 | 实验操作 | 现象 | 解释或结论 |
A | 把SO2通入紫色石蕊试液中 | 紫色先变红后褪色 | SO2具有漂白性 |
B | 向AgCl沉淀中清加KI溶液 | 白色沉淀变为黄色 | 溶度积:AgI比AgCl更小 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变浅 | 反应2NO2 |
D | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
A. AB. BC. CD. D