题目内容
12.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )
| A. | 元素的非金属性:Y>W | |
| B. | 阴离子的还原性:W2->Q- | |
| C. | 离子半径:Y2->Z3+ | |
| D. | Q、W、Y对应的氢化物的沸点逐渐降低 |
分析 由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置,可知X为N,Y为O,Z为Al,W为S,Q为Cl,
A.同主族,原子序数小的非金属性强;
B.同周期,从左向右非金属性增强,非金属性越强,对应阴离子的还原性越弱;
C.具有相同排布的离子,原子序数大的离子半径小;
D.Y的氢化物含氢键,沸点最大;不含氢键的氢化物中相对分子质量大的沸点高.
解答 解:由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置,可知X为N,Y为O,Z为Al,W为S,Q为Cl,
A.同主族,原子序数小的非金属性强,则元素的非金属性:Y>W,故A正确;
B.同周期,从左向右非金属性增强,非金属性Q>W,则阴离子的还原性为W2->Q-,故B正确;
C.具有相同排布的离子,原子序数大的离子半径小,则离子半径:Y2->Z3+,故C正确;
D.Y的氢化物含氢键,沸点最大;不含氢键的氢化物中相对分子质量大的沸点高,则Y、Q、W对应的氢化物的沸点逐渐降低,故D错误;
故选D.
点评 本题考查元素位置、结构与性质,为高频考点,涉及周期表中同周期和同主族元素的性质变化规律等,把握元素的性质、元素化合物性质是解答本题的关键,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
3.下列叙述正确的是( )
| A. | 在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应吸热 | |
| B. | 同温同压下,4Al(s)+3O2(g)═2Al2O3(s)在常温和点燃条件下的△H不同 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-53.7KJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量大于53.7kJ | |
| D. | 需要加热的化学反应一定是吸热反应 |
20.一定条件下,将A、B、C三种物质各1mol通入一个密闭容器中发生反应:2A+B?2C,达到化学反应限度时,B的物质的量可能是( )
| A. | 1.5 mol | B. | 1 mol | C. | 0.5 mol | D. | 0 |
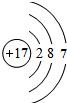
7.某元素二价阴离子的核外有18个电子,质量数为34,该元素的原子核中的中子数为( )
| A. | 16 | B. | 18 | C. | 20 | D. | 22 |
4.在一定的温度下,向CH3COONa的稀溶液里加水稀释,下列各种量变小的是( )
①H+的物质的量浓度
②OH-的物质的量浓度
③c(CH3COO-)/c(CH3COOH)
④c(H+)•c(OH-)
①H+的物质的量浓度
②OH-的物质的量浓度
③c(CH3COO-)/c(CH3COOH)
④c(H+)•c(OH-)
| A. | ①② | B. | ② | C. | ②③ | D. | ②③④ |
 ,NH4Cl的电子式
,NH4Cl的电子式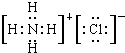 ;
;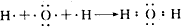 ;
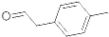
; 是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔(
是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔(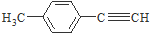 )的一条路线如下:
)的一条路线如下: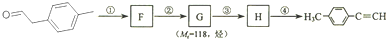
 分子中一定在同一平面的原子数为12个;
分子中一定在同一平面的原子数为12个; 分子中在同一直线上的原子数最多有6个;
分子中在同一直线上的原子数最多有6个;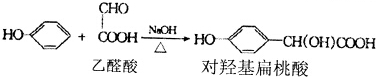
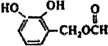 .
.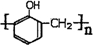 .
.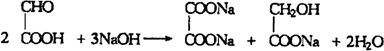 .
.