题目内容
下列叙述中,错误的是( )
| A、苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯 |
| B、苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
| C、甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |
| D、乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 |
考点:苯的性质,乙烯的化学性质
专题:有机反应
分析:A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应,苯中的H被硝基取代,生成硝基苯;
B.碳碳双键与苯环都能与氢气发生加成反应;
C.甲苯与氯气在光照条件下能发生取代反应,只能取代甲基上的氢原子,不能取代苯环上的氢原子;
D.乙烯含有碳碳双键,与溴发生加成反应;
B.碳碳双键与苯环都能与氢气发生加成反应;
C.甲苯与氯气在光照条件下能发生取代反应,只能取代甲基上的氢原子,不能取代苯环上的氢原子;
D.乙烯含有碳碳双键,与溴发生加成反应;
解答:
解:A.苯与浓硝酸在浓硫酸在加热条件下,发生取代反应生成硝基苯与水,反应方程式为 ,故A正确;
,故A正确;
B.苯环在一定条件下能发生加成反应,苯环上连接的碳碳双键易发生加成反应,1摩尔 能与4摩尔氢气发生加成反应,生成乙基环己烷,故B正确;
能与4摩尔氢气发生加成反应,生成乙基环己烷,故B正确;
C.甲苯与氯气在光照条件下能发生取代反应,此时只能取代甲基上的氢原子,不能取代苯环上的氢原子,氢原子的取代是分部同时进行的,一元取代物只取代甲基上的一个氢原子, ,故C错误;
,故C错误;
D.乙烯含有碳碳双键,与溴发生加成反应,化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br,生成1,2-二溴乙烷,故D正确;
故选C.
 ,故A正确;
,故A正确;B.苯环在一定条件下能发生加成反应,苯环上连接的碳碳双键易发生加成反应,1摩尔
 能与4摩尔氢气发生加成反应,生成乙基环己烷,故B正确;
能与4摩尔氢气发生加成反应,生成乙基环己烷,故B正确;C.甲苯与氯气在光照条件下能发生取代反应,此时只能取代甲基上的氢原子,不能取代苯环上的氢原子,氢原子的取代是分部同时进行的,一元取代物只取代甲基上的一个氢原子,
 ,故C错误;
,故C错误;D.乙烯含有碳碳双键,与溴发生加成反应,化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br,生成1,2-二溴乙烷,故D正确;
故选C.
点评:本题考查有机物苯及其同系物的性质,掌握官能团的性质是解答的关键,注意甲苯与氯气在光照条件下只能取代甲基上的氢原子,题目难度中等.

练习册系列答案
相关题目
欲使醋酸溶液中的CH3COO-浓度增大,且不放出气体,可向醋酸中加入少量固体( )
| A、NaOH |
| B、NaHCO3 |
| C、Na2CO3 |
| D、Mg |
一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和○代表不同元素的原子.关于此反应说法错误的是( )


| A、一定属于可逆反应 |
| B、一定属于化合反应 |
| C、一定属于氧化还原反应 |
| D、一定属于放热反应 |
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
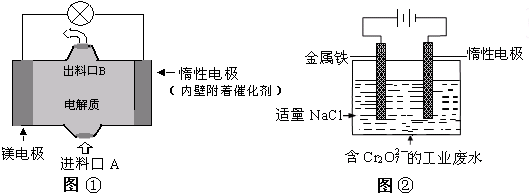

| A、图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B、图②中阳极上的电极反应式为:Fe-3e-═Fe3+ |
| C、图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓ |
| D、若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L氦气中含有的电子数为2NA |
| B、11g的2H218O分子中含NA个中子 |
| C、1mol NH4+离子所含的质子总数为10NA |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
下列类比关系正确的是( )
| A、AlCl3与过量NaOH溶液反应生成[Al(OH)4]-,则与过量NH3?H2O反应也生成[Al(OH)4]- |
| B、Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
| C、Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 |
| D、Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 |
离子方程式H++OH-=H2O可表示的化学方程式是( )
| A、盐酸与氢氧化铜的反应 |
| B、硫酸与氢氧化钠的反应 |
| C、硫酸与氢氧化镁的反应 |
| D、盐酸与氨水的反应 |
在25℃时,用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A、
| ||||
B、
| ||||
C、
| ||||
| D、OH-物质的量 |
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是( )
| A、2H2+O2═2H2O;△H=-142.9kJ/mol |
| B、2H2(g)+O2(g)═2H2O(l);△H=-142.9kJ/mol |
| C、2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l);△H=+571.6kJ/mol |