题目内容
16.下列有关各实验的叙述中正确的是( )| A. | 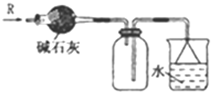 可用于SO2气体的干燥,收集并吸收多余SO2气体,防止SO2逸出污染空气并防止倒吸 可用于SO2气体的干燥,收集并吸收多余SO2气体,防止SO2逸出污染空气并防止倒吸 | |
| B. | 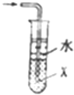 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| C. |  进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集 进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集 | |
| D. | 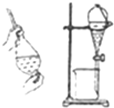 利用氯仿(CHCl3)密度大于乙醇,进行氯仿与乙醇混合物的分离 利用氯仿(CHCl3)密度大于乙醇,进行氯仿与乙醇混合物的分离 |
分析 A.SO2的密度比空气密度大,且与碱石灰反应;
B.苯的密度比水小,不能隔绝气体与水;
C.与氧气反应的气体不能使用排空气法收集,a进气收集密度比空气小的气体,b进气收集密度比空气大的气体;
D.氯仿与乙醇混合物不分层.
解答 解:A.SO2的密度比空气密度大,且与碱石灰反应,则收集及除杂不合理,故A错误;
B.苯的密度比水小,不能隔绝气体与水,则X为苯时不能防止倒吸,应选四氯化碳,故B错误;
C.与氧气反应的气体不能使用排空气法收集,a进气收集密度比空气小的气体,b进气收集密度比空气大的气体,则装置可进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集,故C正确;
D.氯仿与乙醇混合物不分层,不能利用与中分液装置分离,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、气体的收集及防倒吸装置等,把握物质的性质及反应原理为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列分子中所有原子一定处于同一平面的是( )
| A. | CH3CH2CH=CH2 | B. | CH2=CH-CH=CH2 | C. | C6H5-C≡CH | D. | CH3CH=CH2 |
7.常温下,下列对醋酸稀溶液的叙述中,正确的是( )
| A. | 将pH=a的醋酸稀释变为pH=a+1,醋酸的浓度则变为原来的$\frac{1}{10}$ | |
| B. | 将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$变小 | |
| C. | pH=a的醋酸与pH=a+1的醋酸分别中和等物质的量的NaOH溶液,二者所消耗体积比为1:10 | |
| D. | 等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14 |
4.元素周期表里金属元素和非金属元素分界线附近能找到( )
| A. | 新制农药元素 | B. | 制催化剂元素 | ||
| C. | 制半导体元素 | D. | 制耐高温合金元素 |
1.A是一种常见的单质.B.C为常见的化合物.A.B.C均含有元素X.它们有如图所示转化关系(部分产物及反应条件已略去)下列有关推断正确的是( )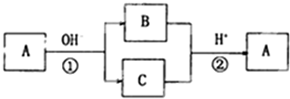
a.X元素为Al;
b.反应①和反应②互为可逆反应;
c.A可能是S或Cl2;
d.反应①和反应②一定是氧化还原反应.

a.X元素为Al;
b.反应①和反应②互为可逆反应;
c.A可能是S或Cl2;
d.反应①和反应②一定是氧化还原反应.
| A. | a和b | B. | c和d | C. | a、b、c、d | D. | b、c、d |
8.下列解释过程或事实的方程式不正确的是( )
| A. | 熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH=Na2SiO3+H2O | |
| B. | 甲醇燃料电池(KOH作电解质溶液)的负极反应式:CH3OH-6e+H2O=CO2+6H+ | |
| C. | 红热的铁丝与水接触,表面形成黑色保护层:3Fe+4H2O=Fe3O4+4H2 | |
| D. | “84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
5.说法正确的是( )
| A. | 含有非极性键的分子一定是非极性分子 | |
| B. | 非极性分子中一定含有非极性键 | |
| C. | 由极性键形成的双原子分子一定是极性分子 | |
| D. | 键的极性与分子的极性无关 |
 实验室中只有0.1000mol•L-1的酸性KMnO4溶液,甲同学用下图所示操作配制100mL0.0010mol•L-1的KMnO4溶液,指出其中的两处错误称取酸性高锰酸钾选用碱式滴定管、在容量瓶稀释浓溶液.
实验室中只有0.1000mol•L-1的酸性KMnO4溶液,甲同学用下图所示操作配制100mL0.0010mol•L-1的KMnO4溶液,指出其中的两处错误称取酸性高锰酸钾选用碱式滴定管、在容量瓶稀释浓溶液.