题目内容
8.下列解释过程或事实的方程式不正确的是( )| A. | 熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH=Na2SiO3+H2O | |
| B. | 甲醇燃料电池(KOH作电解质溶液)的负极反应式:CH3OH-6e+H2O=CO2+6H+ | |
| C. | 红热的铁丝与水接触,表面形成黑色保护层:3Fe+4H2O=Fe3O4+4H2 | |
| D. | “84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
分析 A.二氧化硅为酸性氧化物,能够与碱反应生成盐和水;
B.碱性环境下不能生成氢离子;
C.铁与水蒸气在高温条件下反应生成四氧化三铁和氢气;
D.次氯酸与盐酸发生氧化还原反应生成氯气和是.
解答 解:A.二氧化硅能够与氢氧化钠反应,离子方程式,SiO2+2NaOH=Na2SiO3+H2O,所以熔融烧碱时,不能使用普通石英坩埚,故A正确;
B.甲醇燃料电池(KOH作电解质溶液)的负极反应式,CH3OH-6e-+8OH-═CO32-+6H2O,故B错误;
C.铁与水蒸气在高温条件下反应生成四氧化三铁和氢气,化学方程式为:3Fe+4H2O=Fe3O4+4H2↑,故C正确;
D.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气,离子方程式:ClO-+Cl-+2H+=Cl2↑+H2O,故D正确;
故选:B.
点评 本题考查了化学方程式的书写,明确反应实质是解题关键,注意燃料电池书写电极反应式应考虑电解质,题目难度中等.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
18.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 15g甲基所含有的电子数是10NA个 | |
| B. | 1mol苯乙烯中含有的碳、碳双键数为4NA个 | |
| C. | 标准状况下,1L庚烷所含有的分子数为NA/22.4 | |
| D. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
16.下列有关各实验的叙述中正确的是( )
| A. | 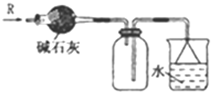 可用于SO2气体的干燥,收集并吸收多余SO2气体,防止SO2逸出污染空气并防止倒吸 可用于SO2气体的干燥,收集并吸收多余SO2气体,防止SO2逸出污染空气并防止倒吸 | |
| B. | 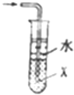 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| C. |  进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集 进行H2,NH3,CO2,Cl,HCl,NO2等气体收集,但不能用于NO气体收集 | |
| D. | 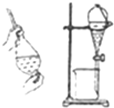 利用氯仿(CHCl3)密度大于乙醇,进行氯仿与乙醇混合物的分离 利用氯仿(CHCl3)密度大于乙醇,进行氯仿与乙醇混合物的分离 |
20.关于[Cr(H2O)4Br2]Br•2H2O的说法正确的是( )
| A. | 配体为水分子,配原子为O,外界为Br- | |
| B. | 中心离子的配位数为6 | |
| C. | 中心离子Cr3+采取sp3杂化 | |
| D. | 中心离子的化合价为+2 |
 .
. A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:
A、B、C是短周期非金属元素,核电荷数依次增大.A原子外围电子排布为ns2np2,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空: