题目内容
9.若用 NA表示阿伏加德罗常数的值,下列叙述不正确的是( )| A. | 在0.1molNaHSO4晶体中阳离子与阴离子总数为0.2NA | |
| B. | 1L0.1mol•L-1的H2SO3溶液中含有H+的数目为0.2NA | |
| C. | 7.8gNa2O2中含有的阴离子数目为0.1NA | |
| D. | 常温常压下,14g乙烯和丙烯的混合气体中氢原子数为2NA |
分析 A、NaHSO4晶体由1个钠离子和1个HSO4-构成;
B、亚硫酸是弱酸,在溶液中不能完全电离;
C、求出过氧化钠的物质的量,然后根据过氧化钠中含1个过氧根来分析;
D、乙烯和丙烯均由CH2构成.
解答 解:A、NaHSO4晶体由1个钠离子和1个HSO4-构成,故0.1molNaHSO4中含0.1mol钠离子和0.1molHSO4-,即阳离子和阴离子共0.2NA个,故A正确;
B、亚硫酸是弱酸,在溶液中不能完全电离,故溶液中的氢离子的个数小于0.2NA个,故B错误;
C、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠中含1个过氧根,故0.1mol过氧化钠中含0.1NA个阴离子,故C正确;
D、乙烯和丙烯均由CH2构成,故14g乙烯和丙烯的混合物中含有的CH2的物质的量为1mol,则含有2NA个氢原子,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.下列金属活动性最强的( )
| A. | Mg | B. | Ag | C. | Cu | D. | Zn |
20.在强碱溶液中,可能大量存在的离子组是( )
| A. | Na+、K+、AlO2-、Cl- | B. | Ba2+、Na+、Al3+、SO42- | ||
| C. | K+、Mg2+、Cl-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
4.亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食能使人中毒.区别食盐和亚硝酸钠的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种有刺激性气味气体的是亚硝酸钠.该气体可能是( )
| A. | NO2 | B. | N2 | C. | NH3 | D. | SO2 |
1.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,28g CO和N2的混合气体中含有的分子总数为NA | |
| B. | 1 mol铁与足量盐酸完全反应时失去的电子数为3NA | |
| C. | 78g过氧化钠晶体中,含2NA个阴离子 | |
| D. | 标准状况下,22.4 LH2S和SO2的混合气体中含有的分子总数为NA |
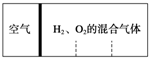 如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的$\frac{1}{4}$)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央.则原来H2、O2的体积之比可能为7:2 或4:5.
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的$\frac{1}{4}$)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央.则原来H2、O2的体积之比可能为7:2 或4:5.