题目内容
80℃时,2L密闭容器中充入0.40molN2O4,发生反应
N2O4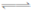 2NO2
2NO2 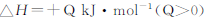 ,获得如下数据:
,获得如下数据: 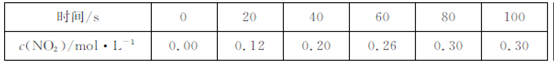 下列判断正确的是
下列判断正确的是
| A.升高温度该反应的平衡常数K减小 |
B.20~40s内,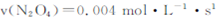 |
| C.反应达平衡时,吸收的热量为0.30QkJ |
| D.100s时再通入0.40molN2O4,达新平衡时N2O4的转化率增大 |
C
解析试题分析: A?该反应为吸热反应,温度升高,平衡向吸热的方向移动,即正反应方向移动,平衡常数K增大,故A错误;B?20~40s 内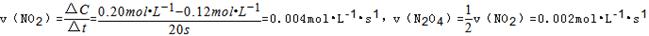 C?浓度不变时,说明反应已达平衡,反应达平衡时,生成NO2的物质的量为0.30mol?L-1×2L=0.60mol,由热化学方程式可知生成2molNO2吸收热量QkJ,所以生成0.6molNO2吸收热量0.3QkJ,故C正确;D?100s时再通入0.40mol N2O4,平衡状态相当于增大压强,平衡逆向移动,N2O4的转化率减小,故D错误;故选C.
C?浓度不变时,说明反应已达平衡,反应达平衡时,生成NO2的物质的量为0.30mol?L-1×2L=0.60mol,由热化学方程式可知生成2molNO2吸收热量QkJ,所以生成0.6molNO2吸收热量0.3QkJ,故C正确;D?100s时再通入0.40mol N2O4,平衡状态相当于增大压强,平衡逆向移动,N2O4的转化率减小,故D错误;故选C.
考点:考查化学反应速率?化学平衡移动以及热量的有关计算

练习册系列答案
相关题目
(14分)从能量的变化和反应的快慢等角度研究反应: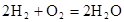 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
| A.使用催化剂 | B.提高氧气的浓度 |
| C.提高反应的温度 | D.降低反应的温度 |
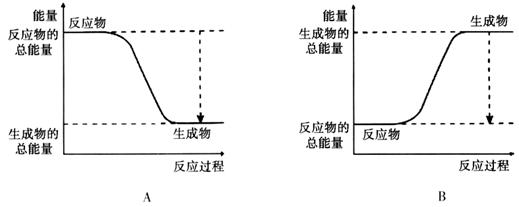
(3)从断键和成键的角度分析上述反应中能量的变化。已知:化学键的键能:
| 化学键 | H—H | O=O | H—O |
键能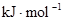 | 436 | 496 | 463 |
(4)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为
(5)氢氧燃料电池的总反应方程式为
 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。 下面关于化学反应的限度的叙述中,正确的是
| A.化学反应的限度都相同 |
| B.可以通过改变温度控制化学反应的限度 |
| C.可以通过延长化学反应的时间改变化学反应的限度 |
| D.当一个化学反应在一定条件下达到限度时,反应即停止 |
把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是
| A.盐酸的浓度 | B.铝条的表面积 | C.溶液的温度 | D.加少量Na2SO4固体 |
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1

 O2(g)=CO2(g) △H2=-283 kJ·mol-1
O2(g)=CO2(g) △H2=-283 kJ·mol-1

 2SO3(g),并达到平衡,在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3(g),并达到平衡,在此过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为