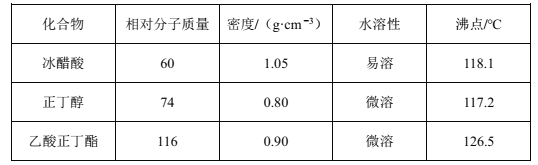
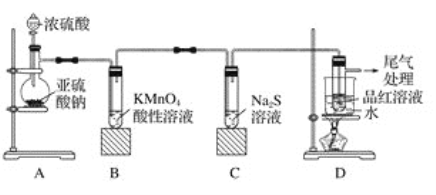
题目内容
【题目】实验室探究SO2性质的装置如图所示。下列说法错误的是( )
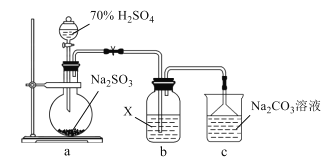
A.装置a中的反应可用铜片和浓硫酸代替
B.若X为H2S溶液,装置b中产生淡黄色沉淀
C.若X为含HCl、BaCl2的FeCl3溶液,装置b中产生白色沉淀
D.反应后装置c中溶液的pH降低
【答案】A
【解析】
A. 铜片和浓硫酸需要加热才能反应生成SO2,故不能替换,故A错误;
B. 若X为H2S溶液,SO2与H2S发生氧化还原反应生成难溶的S,则装置b中产生淡黄色沉淀S,故B正确;
C. FeCl3溶液中Fe3+有氧化性,通入二氧化硫时反应生成硫酸钡沉淀,装置b中产生白色沉淀为硫酸钡,故C正确;
D. 装置c中碳酸钠溶液与二氧化硫反应生成亚硫酸钠溶液,亚硫酸根水解程度小于碳酸根,所以碱性减弱,pH降低,故D正确;
故选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
苯甲酸 | 122 | 122.4 | 249 | 1.3 |
甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4![]() 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
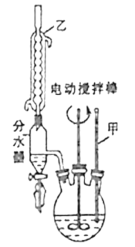
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
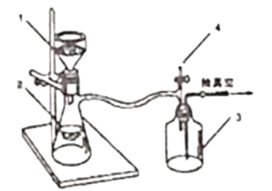
第三步:粗产品用水洗涤2到3次,干燥称量得固体![]() .
.
请回答下列问题:
(1)图1中装置乙的名称为___。
(2)分水器的作用是分离出水其主要目的是___,判断该反应进行完全的实验现象是___。
(3)实验第二步中,趁热过滤的原因是___,采用抽滤的优点是____。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____。
(4)第三步证明粗产品洗涤干净的方法是___。
(5)苯甲酸的产率为____。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。