题目内容
【题目】苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
苯甲酸 | 122 | 122.4 | 249 | 1.3 |
甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
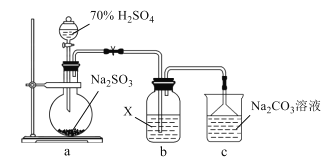
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4![]() 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
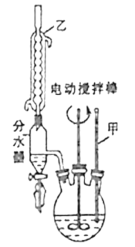
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
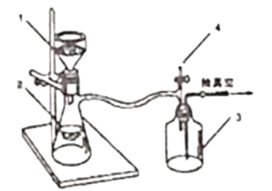
第三步:粗产品用水洗涤2到3次,干燥称量得固体![]() .
.
请回答下列问题:
(1)图1中装置乙的名称为___。
(2)分水器的作用是分离出水其主要目的是___,判断该反应进行完全的实验现象是___。
(3)实验第二步中,趁热过滤的原因是___,采用抽滤的优点是____。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____。
(4)第三步证明粗产品洗涤干净的方法是___。
(5)苯甲酸的产率为____。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
【答案】球形冷凝管 提高甲苯利用率(或转化率) 反应混合液颜色不再发生变化(或反应结束后静置不再分层) 苯甲酸溶解度随温度升高而增大,减少苯甲酸因温度低时析出产率降低 过滤速度快,得到的固体水份少(固液分离更快更彻底) 安全瓶(或防倒吸、平衡气压) 取最后一次的洗涤液少许于试管中,滴加几滴BaCl2溶液,若无沉淀生成,产品洗涤干净 90.2% 用一支干燥洁净的玻璃棒蘸取0.010mol/L的苯甲酸钠溶液滴在pH试纸上,若pH>7,则证明苯甲酸是弱酸
【解析】
(1)回流装置用球形冷凝管;
(2)经冷凝管冷凝回流的冷凝液进入分水器,分层后,甲苯自动流回到三颈烧瓶中,水从分水器中放出去,这样可以促使反应正向进行,提高甲苯的利用率;该反应完成时,三颈烧瓶中酸性KMnO4溶液颜色不再发生变化;
(3)苯甲酸溶解度随温度升高而增大;抽滤具有过滤速率快,得到的固体水分少等优点;从装置图可知,装置3起到安全瓶的作用;
(4)由于第二步用硫酸酸化滤液,因此可通过检验SO42-来判断粗产品是否洗涤干净;
(5)9.2g甲苯的物质的量为:0.1mol,根据反应方程式,理论上生成苯甲酸为:0.1mol,其质量为0.1mol×122g·mol-1=12.2g,根据实际生成11.0g苯甲酸,可求出苯甲酸的产率;
(6)要通过实验确定苯甲酸是弱酸,最简单的方法就是用pH试纸测定0.010mol·L-1苯甲酸钠溶液的pH大小;
(1)乙的名称为球形冷凝管,故答案为:球形冷凝管;
(2)实验过程中,经冷凝管冷凝回流的冷凝液进入分水器,分层后,甲苯自动流回到三颈烧瓶中,生成的水从分水器中放出去,这样可以促使反应正向进行,提高甲苯的利用率,同时能减少抽滤所需时间;该反应完成时,三颈烧瓶中酸性KMnO4溶液颜色不再发生变化,或停止搅拌,静置,液体不再出现分层现象,故答案为:提高甲苯利用率(或转化率);反应混合液颜色不再发生变化(或反应结束后静置不再分层);
(3)苯甲酸溶解度随温度升高而增大,趁热过滤的原因是减少苯甲酸因温度低时析出产率降低;抽滤具有过滤速率快,得到的固体水分少等优点;装置3起到安全瓶(或防倒吸、平衡气压)的作用;故答案为:苯甲酸溶解度随温度升高而增大,减少苯甲酸因温度低时析出产率降低;过滤速度快,得到的固体水份少(固液分离更快更彻底);安全瓶(或防倒吸、平衡气压);
(4)由于第二步用硫酸酸化滤液,因此可通过检验SO42-来判断粗产品是否洗涤干净,检验的方法是向少许最后一次的洗涤液中滴入几滴BaCl2溶液,若无沉淀生成,则说明粗产品洗涤干净,故答案为:取最后一次的洗涤液少许于试管中,滴加几滴BaCl2溶液,若无沉淀生成,产品洗涤干净;
(5)9.2g甲苯的物质的量为:0.1mol,根据反应方程式,理论上生成苯甲酸为:0.1mol,其质量为0.1mol×122g·mol-1=12.2g,根据实际生成11.0g苯甲酸,可求出苯甲酸的产率为11.0g/12.2g×100%≈90.2%,故答案为:90.2%;
(6)实验确定苯甲酸是弱酸,最简单的方法就是用pH试纸测定0.010mol·L-1苯甲酸钠溶液的pH大小,所以用一支干燥洁净的玻璃棒蘸取0.010mol/L的苯甲酸钠溶液滴在pH试纸上,若pH>7,则证明苯甲酸是弱酸,故答案为:用一支干燥洁净的玻璃棒蘸取0.010mol/L的苯甲酸钠溶液滴在pH试纸上,若pH>7,则证明苯甲酸是弱酸。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案