题目内容
4.下列实验操作或记录正确的是( )| A. | 常温常压下测得1molN2的质量为28g | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28mL | |
| C. | 用两只250mL的容量瓶配制0.1mol/L500mL的NaOH溶液 | |
| D. | 用托盘天平称得2.5g胆矾,受热充分失水后,固体质量减轻1.6g |
分析 A.结合m=nM分析;
B.量筒只能读到0.1mL;
C.250mL的容量瓶只能配制250mL溶液;
D.2.5g胆矾,受热充分失水后,减少的质量为水的质量.
解答 解:A.常温常压下测得1mol N2的质量为1mol×28g/mol=28g,故A正确;
B.用量筒测得排水法收集制得的氢气体积可为50.2mL或50.3mL,故B错误;
C.250mL的容量瓶只能配制250mL溶液,配制0.1mol/L 500mL的NaOH溶液,只能选1个500mL容量瓶,故C错误;
D.2.5g胆矾,受热充分失水后,减少的质量为水的质量,即减少质量为2.5g×$\frac{5×18}{250}$=0.9g,故D错误;
故选A.
点评 本题考查化学实验的评价,为基础性习题,涉及物质的量计算、气体的收集、溶液配制及固体称量等,注意常见仪器的使用及感量,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列对分子及性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 由于乳酸(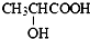 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 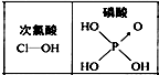 由如图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 |
15.将足量的铜片与20mL 18mol•L-1浓硫酸加热充分反应,收集到标准状况下的二氧化硫气体VL.下列对此反应的有关说法中错误的是( )
| A. | 该反应体现了浓H2SO4的酸性和强氧化性 | |
| B. | 被还原的硫酸为$\frac{V}{22.4}$mol | |
| C. | 反应结束后两种反应物均有剩余 | |
| D. | 参加反应的铜为0.18mol |
12.CaC2和MgC2都是离子化合物,下列叙述中正确的是( )
①CaC2和MgC2都能跟水反应生成乙炔
②CaC2在水中以Ca2+和C22-形式存在
③C22-的电子式
④MgC2的熔点低,可能在100℃以下?
①CaC2和MgC2都能跟水反应生成乙炔
②CaC2在水中以Ca2+和C22-形式存在
③C22-的电子式

④MgC2的熔点低,可能在100℃以下?
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
19.下列表示对应化学反应的离子方程式不正确的是( )
| A. | 用氨水溶解Cu(OH)2:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O | |
| B. | 二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O═SO42-+2Fe2++4H+ | |
| C. | 硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-═NH3•H2O+H2O | |
| D. | 向NaClO溶液中加入浓盐酸:ClO-+Cl-+2H+═Cl2↑+H2O |
9.下列推论正确的是( )
| A. | SiH4的沸点高于CH4,可推测PH3的沸点高于NH3 | |
| B. | CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体 | |
| C. | C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子 | |
| D. | NH4+为正四面体结构,可推测 PH4+ 也为正四面体结构 |
16.下列有关原子结构和元素周期律叙述中不正确的是( )
| A. | 第IA族碱金属元素最高价氧化物的水化物的碱性随原子序数递增而增强 | |
| B. | 第ⅦA族元素是同周期中非金属性最强的元素 | |
| C. | 第ⅦA元素从上到下,其氢化物的稳定性逐渐减弱 | |
| D. | 同周期元素(除0族元素外)从左到右,原子半径和离子半径都逐渐减小 |
13.已知符合分子式为C4H10O的饱和一元醇有4种,那么符合分子式为C5H10O2饱和一元羧酸有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
14.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率( )
| A. | V(H2O)=0.003mol/(L•S) | B. | V(NH3)=0.003mol/(L•S) | ||
| C. | V(NH3)=0.002mol/(L•S) | D. | V(O2)=0.005mol/(L•S) |