题目内容
14.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率( )| A. | V(H2O)=0.003mol/(L•S) | B. | V(NH3)=0.003mol/(L•S) | ||
| C. | V(NH3)=0.002mol/(L•S) | D. | V(O2)=0.005mol/(L•S) |
分析 根据v=$\frac{△c}{△t}$计算v(NO),再根据速率之比等于化学计量数之比,可求出其它物质表示的反应速率.
解答 解:在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则v(NO)=$\frac{\frac{0.3mol}{5L}}{30s}$=0.002mol/(L.s),
速率之比等于化学计量数之比,则:v(H2O)=$\frac{3}{2}$v(NO)=0.003mol/(L.s)
v(NH3)=v(NO)=0.002mol/(L.s),
v(O2)=$\frac{5}{4}$v(NO)=0.0025mol/(L.s),
故选:AC.
点评 本题考查化学反应速率有关计算,常用公式法与速率规律进行计算,根据情况选择合适的方法.

练习册系列答案
相关题目
4.下列实验操作或记录正确的是( )
| A. | 常温常压下测得1molN2的质量为28g | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28mL | |
| C. | 用两只250mL的容量瓶配制0.1mol/L500mL的NaOH溶液 | |
| D. | 用托盘天平称得2.5g胆矾,受热充分失水后,固体质量减轻1.6g |
5.铁单质及其化合物在生活、生产中应用广泛.请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为O2+2H2O+4e-=4OH-.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式表示).在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是酸性环境中,氢离子抑制了铁离子的水解,无法生成氢氧化铁胶体.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO═3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为O2+2H2O+4e-=4OH-.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式表示).在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是酸性环境中,氢离子抑制了铁离子的水解,无法生成氢氧化铁胶体.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO═3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的 金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应 生成氢气 | 高温下氢气能还原氧化 铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形 成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
9.能大量共存于同一种溶液中的一组离子是( )
| A. | Al3+,Cl-,K+,OH- | B. | H+,Na+,SO42-,S2- | ||
| C. | Na+,Ca2+,HCO3-,OH- | D. | Mg2+,H+,SO42-,NO3- |
19.少量铁粉与100mL 0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法的( )
①加H2O ②滴入几滴浓HNO3 ③滴入几滴浓盐酸 ④加少量硫酸铜固体 ⑤加NaCl固体 ⑥升高温度(不考虑盐酸挥发) ⑦改用10mL 0.1mol•L-1盐酸.
①加H2O ②滴入几滴浓HNO3 ③滴入几滴浓盐酸 ④加少量硫酸铜固体 ⑤加NaCl固体 ⑥升高温度(不考虑盐酸挥发) ⑦改用10mL 0.1mol•L-1盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑦ | C. | ③⑥⑦ | D. | ⑤⑥⑦ |
6.下列各组分子中,中心原子均采取sp3不等性杂化的是( )
| A. | PCl3、NH3 | B. | BF3、H2O | C. | CCl4、H2S | D. | BeCl2、BF3 |
3.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| B. | 常温下,在18g18O2中含有NA个氧原子 | |
| C. | 1 mol乙烷中含有C一H的键数为7×6.02×l023 mol-1 | |
| D. | 1mol-OH所含的电子数目为7NA |
4.下列有关物质结构的表述正确的是( )
| A. | 乙酸的比例模型: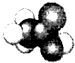 | B. | CO2的电子式: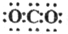 | ||
| C. | 乙醛结构简式:CH3COH | D. | 氯原子的结构示意图: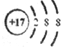 |
 如图是某医院输液用的一瓶葡萄糖注射液标签的部分内容.据此回答以下问题(答案保留2位小数):
如图是某医院输液用的一瓶葡萄糖注射液标签的部分内容.据此回答以下问题(答案保留2位小数):